题目内容
9. 实验室利用过氧化氢溶液和二氧化锰制取氧气的文字表达式为:
实验室利用过氧化氢溶液和二氧化锰制取氧气的文字表达式为:过氧化氢 $\stackrel{二氧化锰}{→}$ 水+氧气.
(1)该反应属于基本反应类型中的分解反应.
(2)为获得氧气,甲、乙、丙三位同学,分别用9g下列物质制备氧气,甲用9g氯酸钾;乙用8g氯酸钾和1g二氧化锰;丙用8g氯酸钾和1g高锰酸钾.右图是乙设计的制取装置图,回答下列问题:
(1)指出装置图的错误之处,并说明错误原因:
①试管口向上倾斜,原因:药品中残存的水分受热变成水蒸气后,在试管口又冷凝成水,回流到热的试管底部,引起试管炸裂;
②伸人试管内的导管太长,原因:不利于赶走管内的空气,影响所得氧气的纯度;
③试管口不宜塞一团棉花,原因:棉花是易燃物,氯酸钾受热分解可使棉花着火燃烧,进而引起爆炸.
(2)写出丙同学制氧气时依次发生的化学反应的文字表达式:
①高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;②氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气.
(3)若装置都正确,完全反应后,三人制得氧气最多的是甲,制取氧气速度最慢的是甲.
(4)收集一瓶氧气,做木炭在氧气中燃烧的实验时,用坩埚钳夹取一小块木炭,在酒精灯上烧至红热,伸入氧气瓶内,烧红的木炭插入氧气瓶里的方法是用坩埚钳夹住木炭从瓶口向下缓慢插入.
分析 制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.图中错误之处:试管口向上倾斜,原因:药品中残存的水分受热变成水蒸气后,在试管口又冷凝成水,回流到热的试管底部,引起试管炸裂;伸人试管内的导管太长,原因:不利于赶走管内的空气,影响所得氧气的纯度;试管口不宜塞一团棉花,原因:棉花是易燃物,氯酸钾受热分解可使棉花着火燃烧,进而引起爆炸.若装置都正确,完全反应后,三人制得氧气最多的是甲,因为氯酸钾的质量是9g;制取氧气速度最慢的是甲,因为甲没有用催化剂;收集一瓶氧气,做木炭在氧气中燃烧的实验时,用坩埚钳夹取一小块木炭,在酒精灯上烧至红热,伸入氧气瓶内,烧红的木炭插入氧气瓶里的方法是用坩埚钳夹住木炭从瓶口向下缓慢插入,是瓶内氧气充分反应.
解答 解:(1)过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,属于分解反应;故答案为:分解反应;
(1)图中错误之处:试管口向上倾斜,原因:药品中残存的水分受热变成水蒸气后,在试管口又冷凝成水,回流到热的试管底部,引起试管炸裂;伸人试管内的导管太长,原因:不利于赶走管内的空气,影响所得氧气的纯度;试管口不宜塞一团棉花,原因:棉花是易燃物,氯酸钾受热分解可使棉花着火燃烧,进而引起爆炸;故答案为:①试管口向上倾斜,原因:药品中残存的水分受热变成水蒸气后,在试管口又冷凝成水,回流到热的试管底部,引起试管炸裂;②伸人试管内的导管太长,原因:不利于赶走管内的空气,影响所得氧气的纯度;③试管口不宜塞一团棉花,原因:棉花是易燃物,氯酸钾受热分解可使棉花着火燃烧,进而引起爆炸.
(2)高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,要注意配平;故答案为:①高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气,②氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气.
(3)若装置都正确,完全反应后,三人制得氧气最多的是甲,因为氯酸钾的质量是9g;制取氧气速度最慢的是甲,因为甲没有用催化剂;故答案为:甲 甲.
(4)收集一瓶氧气,做木炭在氧气中燃烧的实验时,用坩埚钳夹取一小块木炭,在酒精灯上烧至红热,伸入氧气瓶内,烧红的木炭插入氧气瓶里的方法是用坩埚钳夹住木炭从瓶口向下缓慢插入,是瓶内氧气充分反应;故答案为:坩埚钳;用坩埚钳夹住木炭从瓶口向下缓慢插入.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了文字表达式的书写和注意事项等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| A. | 反应后溶液质量一定增加 | B. | M可能是铁 | ||
| C. | M表面有固体析出 | D. | M的活动性比Ag弱 |
| A. | 原子核由质子和电子构成 | |
| B. | 化学变化中原子不能再分而分子可以 | |
| C. | 中子不带电,质子带负电,电子带正电 | |
| D. | 相对原子质量=质子数+电子数 |
| A. |  稀释浓硫酸 | B. |  测液体的pH值 | C. |  称取10.5克NaCl | D. |  熄灭酒精灯 |
 如图表示的是单质、化合物、含氧化物、氧化物之间的包含与不包含关系,若大园代表纯净物,则“1”、“4”依次表示上述物质中的单质、氧化物.
如图表示的是单质、化合物、含氧化物、氧化物之间的包含与不包含关系,若大园代表纯净物,则“1”、“4”依次表示上述物质中的单质、氧化物.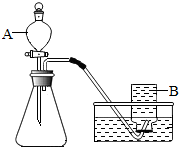 某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.
某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.