题目内容
15.将黄铜(铜锌合金)32.5g放入足量的100g稀硫酸中,完全反应后,剩余物的质量为132.3g,求黄铜中铜的质量分数.分析 烧杯中总物质前后减少的质量为氢气的质量,利用锌和硫酸反应的化学方程式,根据氢气的质量求出锌的质量,进而求出铜的质量,最后根据 $\frac{铜的质量}{黄铜的质量}$×100%求出黄铜中铜的质量分数.
解答 解:氢气的质量=32.5g+100g-132.3g=0.2g.
设锌的质量为x.
Zn+H2SO4=ZnSO4+H2↑
65 2
x 0.2g
$\frac{65}{x}=\frac{2}{0.2g}$
x=6.5g
黄铜中铜的质量分数:$\frac{32.5g-6.5g}{32.5g}$×100%=80%
答:黄铜中铜的质量分数为80%.
点评 利用质量守恒定律,根据反应前后质量差计算出放出氢气质量为解决问题的出发点.

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
5.以下是空气污染指数与质量级别、质量状况的对应关系:
世博会期间,上海市民可提前2天获知空气质量情况.2010年9月1日,上海市区的空气污染指数为48,首要污染物为:可吸入颗粒物.根据以上信息,判断上海市区当天的空气质量级别和空气质量状况分别是( )
| 污染指数 | 50以下 | 51~100 | 101~200 | 201~300 | 301以上 |
| 质量级别 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ |
| 质量状况 | 优 | 良 | 轻度污染 | 中度污染 | 重度污染 |
| A. | Ⅰ级 优 | B. | Ⅱ级 良 | C. | Ⅲ级 轻度污染 | D. | Ⅴ级 重度污染 |
6.山梨酸(C6H8O2)是国际粮农、卫生组织推荐的高效安全防腐保鲜剂.下列有关山梨酸的描述正确的是( )
| A. | 碳、氢、氧的元素质量比为72:8:32 | |
| B. | 由6个碳原子、8个氢原子和2个氧原子构成 | |
| C. | 山梨酸中碳元素的质量分数为72% | |
| D. | 1个山梨酸分子中含有1个氧分子 |
4.准确量取20mL蒸馏水,应选择的一组仪器是( )
| A. | 50mL量筒 | B. | 20mL量筒和胶头滴管 | ||
| C. | 10mL量筒和胶头滴管 | D. | 100mL量筒 |

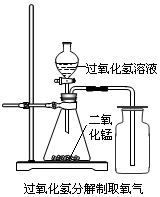 实验室中,常采用分解过氧化氢溶液(二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.
实验室中,常采用分解过氧化氢溶液(二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.