题目内容
在做“氢气还原氧化铜”的实验中,将8g氧化铜放入试管中,通入足量的氢气并加热一段时间.再次称量固体时,发现剩余固体的质量为7.2g,问生成铜的质量为多少?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据氢气和氧化铜在加热的条件下生成铜和水,固体减少的质量是氧元素的质量,然后结合化学方程式进行解答.
解答:解:通过分析题意可知,固体减少质量为:8-7.2=0.8g,
设生成铜的质量为x,
CuO+H2
Cu+H2O 固体减少
80 64 16
x 0.8g
=
x=3.2g
答:生成铜的质量为3.2g.
设生成铜的质量为x,
CuO+H2
| ||
80 64 16
x 0.8g
| 64 |
| x |
| 16 |
| 1.8g |
x=3.2g
答:生成铜的质量为3.2g.
点评:通过分析得出固体质量减少的质量即为参加反应氧化铜中氧元素质量,此为解答本问题的基础.

练习册系列答案
相关题目
如图,下列说法正确是( )
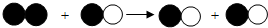
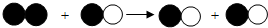
| A、生成物一定是混合物 |
| B、分子在化学变化中不可分 |
| C、化学反应前后原子的种类不变 |
| D、该反应既不是化合反应也不是分解反应 |
下列变化属于化学变化的是( )
| A、西瓜榨成汁 | B、木炭燃烧 |
| C、石蜡熔化 | D、钢丝球刷碗 |
质量守恒定律是帮助我们认识化学反应实质的重要理论,在化学反应aA+bB=cC+dD中,下列说法正确的是( )
| A、化学计量数a与b之和一定等于c与d之和 |
| B、若取xgA和xgB反应,生成C和D的质量总和不一定是2xg |
| C、反应物A和B的质量比一定等于生成物C和D的质量比 |
| D、若A和C有一种是氧气,则该反应一定是化合反应 |
 ”和“
”和“ ”表示两种不同原子.
”表示两种不同原子.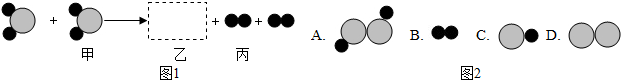
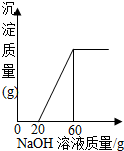 向由40g盐酸和一定质量的硫酸铜溶液组成的混合溶液中慢慢滴入20%的氢氧化钠溶液并振荡,所加氢氧化钠溶液的质量与生成沉淀的质量关系如图所示.求算:
向由40g盐酸和一定质量的硫酸铜溶液组成的混合溶液中慢慢滴入20%的氢氧化钠溶液并振荡,所加氢氧化钠溶液的质量与生成沉淀的质量关系如图所示.求算: