题目内容
实验室制氧气的方法有好几种,加热氯酸钾和二氧化锰的固体混合物可制得氧气(氯酸钾能溶于水,反应后生成物除了氧气还有氯化钾,氯化钾能溶解于水二氧化锰不溶于水),为了证明其中二氧化锰是反应的催化剂,可以设计加热氯酸钾和氯酸钾与二氧化锰的混合物两个对比实验,比较生成氧气速率的大小.试回答下列问题:
(1)进行对比实验可用带火星的木条来检查生成的氧气,若不用带火星的木条,你还能用什么简单的方法来检查生成氧气的速率大小呢?请简单叙述你的方法和所观察到的现象: .
(2)若要进一步证明二氧化锰是反应的催化剂而不是一般的反应物,在上述的实验中还要用到托盘天平,其作用是 .
为了从反应后的固体残渣中得到干燥的二氧化锰固体,需要依次经过的溶解、 和洗涤、 四步主要步骤.
(1)进行对比实验可用带火星的木条来检查生成的氧气,若不用带火星的木条,你还能用什么简单的方法来检查生成氧气的速率大小呢?请简单叙述你的方法和所观察到的现象:
(2)若要进一步证明二氧化锰是反应的催化剂而不是一般的反应物,在上述的实验中还要用到托盘天平,其作用是
为了从反应后的固体残渣中得到干燥的二氧化锰固体,需要依次经过的溶解、
考点:催化剂的特点与催化作用,混合物的分离方法
专题:空气与水
分析:(1)根据氧气生成速率的检验方法,因为氧气不溶于水,可以通过观察导管口是否有连续气泡来判断氧气生成速率大小解答.
(2)根据催化剂特点及混合物的分离方法解答;催化剂在化学反应前后质量和化学性质不发生变化,分离可溶物与不溶物而最终要获得不溶物的步骤依次包括:溶解、过滤、洗涤、烘干.
(2)根据催化剂特点及混合物的分离方法解答;催化剂在化学反应前后质量和化学性质不发生变化,分离可溶物与不溶物而最终要获得不溶物的步骤依次包括:溶解、过滤、洗涤、烘干.
解答:解:
(1)因为氧气不溶于水,所以可通过给试管塞上带导管的塞子,把试管放入水中的方法来检验氧气生成速率,进而通过观察导管口是否有连续气泡判断氧气生成速率大小.
(2)因为催化剂在化学反应前后质量和化学性质不发生变化,故答案为:称量反应前后二氧化锰质量;分离可溶物与不溶物而最终要获得不溶物的步骤依次包括:溶解、过滤、洗涤、烘干.
答案:
(1)给试管塞上带导管的塞子,把导管放入水中,通过观察导管口是否有连续气泡判断氧气生成速率大小
(2)称量反应前后二氧化锰质量 过滤 烘干
(1)因为氧气不溶于水,所以可通过给试管塞上带导管的塞子,把试管放入水中的方法来检验氧气生成速率,进而通过观察导管口是否有连续气泡判断氧气生成速率大小.
(2)因为催化剂在化学反应前后质量和化学性质不发生变化,故答案为:称量反应前后二氧化锰质量;分离可溶物与不溶物而最终要获得不溶物的步骤依次包括:溶解、过滤、洗涤、烘干.
答案:
(1)给试管塞上带导管的塞子,把导管放入水中,通过观察导管口是否有连续气泡判断氧气生成速率大小
(2)称量反应前后二氧化锰质量 过滤 烘干
点评:此题考查了氧气的检验、混合物的分离方法及催化剂的特点等,需要同学们熟练掌握.

练习册系列答案
相关题目
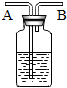 如图所示装置,有洗气、储气等用途.在医院给病人输氧气时,也利用了类似的装置,并在装置中盛放适量蒸馏水.以下说法不正确的是( )
如图所示装置,有洗气、储气等用途.在医院给病人输氧气时,也利用了类似的装置,并在装置中盛放适量蒸馏水.以下说法不正确的是( )| A、该装置可为病人供给相对湿润的氧气. |
| B、导管 B 连接病人吸氧气的塑胶管 |
| C、该装置可用来观察输出氧气的速度 |
| D、该装置可用来调节输出氧气的速度 |
逻辑推理是一种重要的化学思维方法,以下推理合理的是( )
| A、因为H2O和H2O2的组成元素相同,所以它们的化学性质相同 |
| B、因为蜡烛燃烧生成CO2和H2O,所以蜡烛组成里一定含有C和H |
| C、离子是带电的原子或原子团,所以带电的粒子就是离子 |
| D、因为氧化物一定含氧元素,所以含有氧元素的物质一定是氧化物 |
下列说法正确的是( )
A、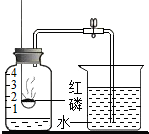 测定空气中氧气含量,可以用硫粉代替红磷 |
B、 用灯帽可以该灭酒精灯,是因为隔开了氧气 |
C、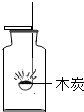 木炭在氧气中燃烧,产生明亮的蓝色火焰 |
D、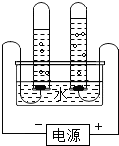 电解水时加入少量稀硫酸是催化剂 |
下面四位同学的做法符合实验室规则的是( )
| A、小明做实验太投入,让同学帮带午饭在实验室里面吃 |
| B、小雪进实验室做氧气的性质实验时,做完一个,再到处找下一个实验所需的仪器和药品 |
| C、小刚做完实验后,看到剩余的药品无毒,就直接倒入了下水道中 |
| D、小轩实验完毕后,将所用器皿洗涤干净,放回规定的位置 |