题目内容
如图1所示是氢氧化钠溶液与盐酸反应的实验研究.
(1)未滴加盐酸时,烧杯中溶液呈 色.
(2)随着盐酸不断滴入,烧杯中溶液的pH逐渐 (填“增大”、“减小”或“不变”),该反应的化学方程式是 .
(3)随着盐酸不断滴入,烧杯中溶液温度变化如坐标图2所示.某时刻测得溶液的温度是32℃,请判断b点时溶液的酸碱性并说明理由 .
(4)当溶液的温度为38℃时,可证明溶液不含氢氧化钠的实验方法是 (填选项).
A.品尝烧杯中溶液的味道
B.用手沾取烧杯中溶液并体验是否有滑腻感
C.往烧杯中再滴加少量氢氧化钠溶液并观察溶液颜色.
考点:
中和反应及其应用;碱的化学性质;溶液的酸碱性与pH值的关系.
专题:
常见的酸 酸的通性.
分析:
(1)根据酚酞试液在碱性溶液中的变色情况来分析;
(2)根据稀盐酸能与氢氧化钠发生中和反应来分析;
(3)根据到达b点的温度变化来分析;
(4)根据氢氧化钠的性质来分析.
解答:
解:(1)氢氧化钠溶液是一种碱性溶液能使无色酚酞试液变红色;故填:红;
(2)随着滴入稀盐酸,氢氧化钠与稀盐酸发生中和反应生成氯化钠和水,盐酸显酸性,随着盐酸的滴加,溶液的碱性减弱,酸性增强,pH变小;故填:减小;NaOH+HCl=NaCl+H2O;
(3)b点的温度是由高到低的趋势,说明是中和反应恰好完成后,继续滴加稀盐酸到过量,故填:酸性,因为是溶液的温度由高到降低;
(4)A.在实验室中不能品尝试剂的味道;
B.此液体具有腐蚀性,不能用手直接接触;
C.往烧杯中再滴加少量氢氧化钠溶液并观察瞬间溶液颜色变化,若先变红,后变无色,证明其中没有氢氧化钠.
故选C.
点评:
本题考查了中和反应过程中的热量变化,完成此题,可以依据已有的知识以及图象进行.

根据如图所示实验,判断下列说法 的是( )
的是( )

|
| A. | 浓盐酸有挥发性 | B. | HCl分子在运动 |
|
| C. | Y杯溶液的颜色会改变 | D. | Y杯内发生了置换反应 |
话说“不是一家人,不进一家门”,我是NaOH溶液,我的家人和谐共处,相互间不发生反应.以下溶液中能进我家门的一组是( )
|
| A. | KNO3、Na2SO4、HCl、KCl | B. | KNO3、NaCl、NH4Cl、Na2SO4 |
|
| C. | KOH、BaCl2、KCl、NaNO3 | D. | K2CO3、K2SO4、CaCl2、NaNO3 |
向一定量4%的氢氧化钠溶液中逐滴加入稀盐酸,有关分析错误的是( )
|
| A. |
| B. |
| C. |
| D. |
|
如图是甲、乙两位同学一起在实验室进行的氢氧化钠与盐酸中和反应的实验.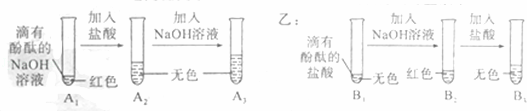
(说明:图中A1、A2、A3、B1、B2、B3均为溶液编号)
根据图中实验,请你与甲、乙同学一起完成下列探究:
| 探究环节 | 甲同学的探究 | 乙同学的探究 |
| 提出问题 | A3溶液为什么不变红? | B3溶液中溶质成分是什么?(酚酞不计) |
| 做出猜想 | 实验过程中,酚酞变质了? | 猜想一:NaCl 猜想二:NaCl HCl |
| 实验验证 | (1)取少量A3溶液于另一试管中,向其中滴加NaOH溶液,溶液变红,说明甲同学的猜想 (填“成立”或“不成立”) (2)你认为,在常温下A2溶液测出的pH 应 (填“>”、“=”或“<”)7 | 取少量B2溶液加入盛有少量铁粉的试管中,观察到有无色气泡产生,固体逐渐减少,溶液由无色变 ,据此,你认为乙同学的猜想 (填“一”或“二”)成立 |
| 交流反思 | (1)甲、乙同学的实验中,反应均涉及到的化学方程式是 . (2)A3溶液未变红,你认为原因是A2溶液中 较多,加入的NaOH溶液未将其完全中和. (3)甲、乙同学经过实验对比探究,一致认为做化学实验时应注意药品用量的控制. |








 则100吨这样的菱锌矿理论上最多制得锌多少吨?(写出计算过程)
则100吨这样的菱锌矿理论上最多制得锌多少吨?(写出计算过程)