题目内容
如图是甲、乙两位同学一起在实验室进行的氢氧化钠与盐酸中和反应的实验.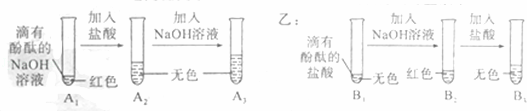
(说明:图中A1、A2、A3、B1、B2、B3均为溶液编号)
根据图中实验,请你与甲、乙同学一起完成下列探究:
| 探究环节 | 甲同学的探究 | 乙同学的探究 |
| 提出问题 | A3溶液为什么不变红? | B3溶液中溶质成分是什么?(酚酞不计) |
| 做出猜想 | 实验过程中,酚酞变质了? | 猜想一:NaCl 猜想二:NaCl HCl |
| 实验验证 | (1)取少量A3溶液于另一试管中,向其中滴加NaOH溶液,溶液变红,说明甲同学的猜想 (填“成立”或“不成立”) (2)你认为,在常温下A2溶液测出的pH 应 (填“>”、“=”或“<”)7 | 取少量B2溶液加入盛有少量铁粉的试管中,观察到有无色气泡产生,固体逐渐减少,溶液由无色变 ,据此,你认为乙同学的猜想 (填“一”或“二”)成立 |
| 交流反思 | (1)甲、乙同学的实验中,反应均涉及到的化学方程式是 . (2)A3溶液未变红,你认为原因是A2溶液中 较多,加入的NaOH溶液未将其完全中和. (3)甲、乙同学经过实验对比探究,一致认为做化学实验时应注意药品用量的控制. |
考点:
中和反应及其应用;酸的化学性质;碱的化学性质;溶液的酸碱性与pH值的关系;书写化学方程式、文字表达式、电离方程式.
专题:
科学探究.
分析:
甲:
(1)根据加酸进行中和反应,变成中性然后变成酸性,取少量A3溶液于另一试管中,向其中滴加NaOH溶液,溶液变红,说明酚酞溶液没有变质解答;
(2)根据A3溶液为不变红,可能是A2溶液中盐酸较多,加入的NaOH溶液未将其完全中和解答;
乙:根据铁可以和酸反应解答;
根据反应物和生成物书写化学反应方程式,
解答:
解:加酸进行中和反应,变成中性然后变成酸性,既然原溶液显碱性所以酚酞的颜色开始是红色的,加酸后,红色会逐渐的褪去;
甲:(1)取少量A3溶液于另一试管中,向其中滴加NaOH溶液,溶液变红,说明酚酞溶液没有变质,说明甲同学的猜想不成立;
(2)A3溶液为不变红,可能是A2溶液显酸性,在常温下A2溶液测出的pH 应小于7;
乙:取少量B2溶液加入盛有少量铁粉的试管中,观察到有无色气泡产生,固体逐渐减少,溶液由无色变浅绿色,据此,乙同学的猜想二成立;
该反应是氢氧化钠和盐酸发生中和反应生成氯化钠和水,故答案为:NaOH+HCl=NaCl+H2O,
A3溶液为不变红,可能是A2溶液中盐酸较多,加入的NaOH溶液未将其完全中和,.
答案:
| 究环节 | 甲同学的探究 | 乙同学的探究 |
| 提出问题 | A3溶液为什么不变红? | B3溶液中溶质成分是什么?(酚酞不计) |
| 做出猜想 | 实验过程中,酚酞变质了? | 猜想一:NaCl 猜想二:NaCl HCl |
| 实验验证 | (1)取少量A3溶液于另一试管中,向其中滴加NaOH溶液,溶液变红,说明甲同学的猜想 不成立(填“成立”或“不成立”) (2)你认为,在常温下A2溶液测出的pH 应<(填“>”、“=”或“<”)7 | 取少量B2溶液加入盛有少量铁粉的试管中,观察到有无色气泡产生,固体逐渐减少,溶液由无色变 浅绿色,据此,你认为乙同学的猜想 二(填“一”或“二”)成立 |
| 交流反思 | (1)甲、乙同学的实验中,反应均涉及到的化学方程式是 NaOH+HCl=NaCl+H2O. (2)A3溶液未变红,你认为原因是A2溶液中 盐酸较多,加入的NaOH溶液未将其完全中和. (3)甲、乙同学经过实验对比探究,一致认为做化学实验时应注意药品用量的控制. |
点评:
要想解答好这类题目,首先,要理解和熟记中和反应及其应用等相关知识.然后,根据所给的实验、问题情景等,结合所学的相关知识和技能,以及自己的生活经验所得,细致地分析题意等各种信息资源,联系起来综合分析,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.

 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案下图是实验室制取气体的一些装置,据图回答有关问题。
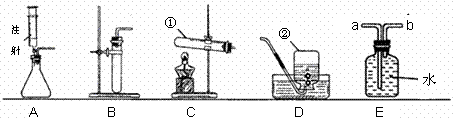 |
(1)写出指定仪器的名称:① ;② ;
(2)写出一个实验室用装置B制取气体的反应的化学方程式 ;
(3)实验室在常温下用块状电石与水反应制取乙炔气体,该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂。你认为上图中最适合制取乙炔气体的发生装置是
(填装置序号);如果用E图所示装置收集乙炔,气体应从 (填“a”或“b”)端管口通入。
根据图,判断以下说法错误的是( )

|
| A. | 取液后的滴管不能倒置 |
|
| B. | 用玻璃棒搅拌使反应充分 |
|
| C. | 用酚酞溶液判断该反应是否发生 |
|
| D. | 生成盐和水的反应都是中和反应 |
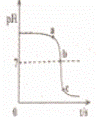
某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示,下列说法正确的是( )
|
| A. | 图中c点所示溶液呈碱性 |
|
| B. | 图中a点所示溶液中,含有的溶质是Na2SO4和H2SO4 |
|
| C. | 该实验是将氢氧化钠溶液逐滴滴入到盛有硫酸的烧杯中 |
|
| D. | 由a点到b点的pH变化过程证明酸和碱发生了中和反应 |
空气中氮气的含量最多,氮气在高温、高能量条件下可与某些物质发生反应。下图是以空气和其他必要的原料合成氮肥(NH4NO3)的工业流程。请按要求回答下列问题:
 (1)步骤①中发生的是________变化(填“物理”或“化学”)。
(1)步骤①中发生的是________变化(填“物理”或“化学”)。
(2)写出步骤③中发生反应的化学方程式_________________________________。
(3)上述化学反应中属于化合反应的有________个。
(4)右图是化肥硝酸铵包装袋上的部分说明:
硝酸铵应具有的性质是 (填字母)。
A.易溶于水 B.有挥发性 C.受热易分解
施用该类肥料时,要避免与碱性物质混合使用,写出硝酸铵与
熟石灰反应的化学方程式__________________________________。
|
不锈钢材料中含有的金属铬(Cr)能提高钢的抗氧化性和耐腐蚀性.为了解金属铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,小娟与小涛进行了如下探究活动.
【猜想和假设】根据所学知识,猜想三种金属在金属活动顺序中的相对位置关系:
猜想一:Cr Al Cu 猜想二:Al Cr Cu 猜想三:
【实验和探究】
(1)小娟的实验:取大小相同的铝、铬、铜三种金属片(用砂纸打磨光亮)
| 实验步骤 | 实验现象 | 解释与结论 |
| 分别取三支试管,向其中入 等质量、等浓度的稀硫酸然 后将铝、铬、铜三种金属分 别插入三支试管中. | 铝片表面产生的气泡较快; 铬片表面产生气泡较缓慢, 溶液变蓝色; 铜片无明显现象. | 猜想 成立. 铬与稀硫酸反应生成蓝色的 硫酸亚铬(CrSO4)溶液,该反应的化学方程式为 . |
(2)小涛的实验:
小涛只选用了三种药品进行实验,也得出了三种金属在金属活动顺序中的相对位置关系.则他选用的三种药品可能是 .
【总结与归纳】由上述实验得出比较金属活动性强弱的方法有:① ;② .

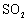 ,还能将其转化为石膏(
,还能将其转化为石膏(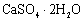 )等产品,实现“变废为宝”。主要物质转化关系如下:
)等产品,实现“变废为宝”。主要物质转化关系如下: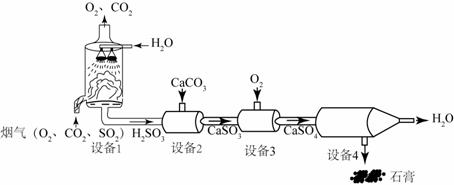
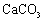 的目的是将
的目的是将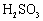 转化为 。
转化为 。