题目内容
3.甲烷和水反应可以制水煤气,其反应的微观示意图如图所示:
下列对该反应的叙述正确的是( )
| A. | 一个甲分子中含有4个原子 | B. | 反应前后元素种类改变 | ||
| C. | 反应前后分子数目不变 | D. | 该反应中,丙和丁的质量比为14:3 |
分析 根据反应的微观示意图分析,反应物是甲烷和水,生成物是一氧化碳和氢气,反应的化学方程式为CH4+H2O $\frac{\underline{\;一定条件\;}}{\;}$CO+3H2,据方程式的意义分析解答即可.
解答 解:由图示可知,该反应的反应物是甲烷和水,生成物是一氧化碳和氢气,反应的化学方程式为:CH4+H2O $\frac{\underline{\;一定条件\;}}{\;}$CO+3H2.
A、由甲烷的分子构成可知,一个甲分子中含有5个原子,故错;
B、由微粒的变化可知,反应前后原子的种类不变,元素的种类也不变,故错;
C、由反应的化学方程式可知,每2个分子变化成了4个分子,反应前后分子数目发生了变化,故错;
D、由上述方程式可知,该反应中,丙和丁的质量比为28:(2×3)=14:3,故正确.
故选D.
点评 本题主要考查了化学反应中微观粒子方面的知识,明确每个模型表示的含义,这是解决这类题目的关键.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
13.下列实验操作正确的是( )
| A. | 实验桌上酒精着火立即用水浇灭 | |
| B. | 实验室制取氯化氢气体时,用排水法收集 | |
| C. | 测定溶液酸碱度时,将pH试纸直接放入待测液中 | |
| D. | 配制稀硫酸时,将浓硫酸倒入水中,并用玻璃棒不断搅拌 |
18.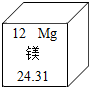 元素周期表中,镁元素的信息如图所示,对图中信息解释不正确的是( )
元素周期表中,镁元素的信息如图所示,对图中信息解释不正确的是( )
 元素周期表中,镁元素的信息如图所示,对图中信息解释不正确的是( )
元素周期表中,镁元素的信息如图所示,对图中信息解释不正确的是( )| A. | 核外电子数为 24 | B. | 原子序数为12 | ||
| C. | 元素符号为Mg | D. | 相对原子质量为24.31 |
8.同学们来到了“自制酸碱指示剂”展台.
(1)上述两种植物的汁液不适合做酸碱指示剂的是胡萝卜.
(2)将紫甘蓝汁液滴入稀硫酸中,溶液呈红 色.
| 植物的汁液 | 白醋 | 蒸馏水 | 氢氧化钠溶液 |
| 紫甘蓝 | 红色 | 蓝紫色 | 绿色 |
| 胡萝卜 | 橙色 | 橙色 | 橙色 |
(2)将紫甘蓝汁液滴入稀硫酸中,溶液呈红 色.
15.氢氧化钙常用于改良酸性土壤,其俗称为( )
| A. | 生石灰 | B. | 大理石 | C. | 石灰石 | D. | 熟石灰 |
12.工业烟气脱硫就是将烟气中含有的二氧化硫除去.采用“双碱法”脱硫的工业流程如图.
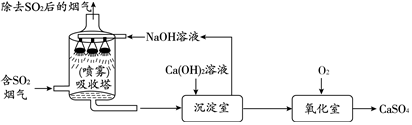
(1)吸收塔中,用NaOH溶液吸收SO2生成亚硫酸钠(Na2SO3)和水,NaOH溶液喷成雾状能充分吸收SO2的原因是增大吸收面积.
(2)沉淀室中发生的是复分解反应,化学方程式为Na2SO3+Ca(OH)2═CaSO3↓+2NaOH.
(3)氧化室中,化学反应的基本类型是化合反应.
(4)已知部分原料的价格如表所示.
上述工业流程中,处理相同量的SO2,双碱法所需的原料成本比用NaOH直接吸收更低,原因是实现了NaOH的循环利用,减少了NaOH的用量.

(1)吸收塔中,用NaOH溶液吸收SO2生成亚硫酸钠(Na2SO3)和水,NaOH溶液喷成雾状能充分吸收SO2的原因是增大吸收面积.
(2)沉淀室中发生的是复分解反应,化学方程式为Na2SO3+Ca(OH)2═CaSO3↓+2NaOH.
(3)氧化室中,化学反应的基本类型是化合反应.
(4)已知部分原料的价格如表所示.
| 试剂 | Ca(OH)2 | NaOH |
| 价格(元/kg) | 0.36 | 2.90 |
2.蒸馒头、炸油条时常用到一种白色物质,它既能中和面粉发酵过程产生的酸,又能起发泡作用,这种白色物质是( )
| A. | NaOH | B. | Ca(OH)2 | C. | NaHCO3 | D. | NaCl |