题目内容
5.长期盛放石灰水的试剂瓶内壁有一白色物质:①这层白色物质是CaCO3,形成原因的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;
②用稀盐酸除去,有关化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑.
分析 长期盛放石灰水的试剂瓶内壁有一白色物质,说明生成了不溶物,且是与空气中某些成分反应,可据此答题.石灰水的主要成分是Ca(OH)2,Ca(OH)2可与空气中的CO2反应生成CaCO3,其反应方程式为CO2+Ca(OH)2=CaCO3↓+H2O,CaCO3是一种白色物质,不溶于水,故内壁有白色物质;CaCO3可与稀盐酸反应生成CaCl2、H2O和CO2,故可用稀盐酸来去除.
解答 解:(1)石灰水的成分是Ca(OH)2,与空气中的二氧化碳发生反应可生成碳酸钙,
反应方程式为CO2+Ca(OH)2=CaCO3↓+H2O,CaCO3是一种白色物质,不溶于水,故内壁有白色物质.
(2)CaCO3是一种白色物质,不溶于水,但可与稀盐酸反应生成CaCl2、H2O和CO2,
反应方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
故答案为:①CaCO3;CO2+Ca(OH)2=CaCO3↓+H2O
②稀盐酸;CaCO3+2HCl=CaCl2+H2O+CO2↑.
点评 此题主要考查CaCO3的一些化学性质,通过分析变化现象确定物质,还需学生熟练写方程式.

练习册系列答案
相关题目
11.关于“粗盐提纯”实验的说法中,正确的是( )
| A. | 称量时,先将盛有粗盐的烧杯放在电子天平上进行“去皮”操作 | |
| B. | 蒸发操作中,玻璃棒搅拌溶液的主要作用是防止飞溅 | |
| C. | 主要操作步骤是:计算、称量、量取、过滤 | |
| D. | 过滤时要用到的仪器、用品是:滤纸、铁架台、量筒 |
12.石墨烯是从石墨中分离出来的单原子层石墨,它具有超强导电、导热的性能.下列关于石墨烯的说法中,不正确的是( )
| A. | 属于一种新型的化合物 | B. | 可做散热材料 | ||
| C. | 可做新型电池的电极 | D. | 在一定条件下能与氧气反应 |
9.根据某燃料X完全燃烧的化学方程式:X+3O2$\stackrel{点燃}{→}$2CO2+3H2O,判断错误的是( )
| A. | X的化学式为C2H6O | |
| B. | X是有机物 | |
| C. | 化学方程式中各物质的系数比与物质的量之比相等 | |
| D. | 该反应前后分子的个数没有发生改变 |
14.下列有关元素的叙述正确的是( )
| A. | 质子数相同的两种粒子一定属于同种元素 | |
| B. | 同种元素的原子结构和质量完全相同 | |
| C. | 元素的种类是由核内质子数决定的 | |
| D. | 元素是具有相同中子数的一类原子的总称 |
15.如表是KNO3、NaCl在不同温度下的部分溶解度数据,请回答问题:
①10℃时,NaCl溶解度是35.8g.
②在20℃时,将50克硝酸钾溶解在100克水中,形成的是饱和(填“饱和”或“不饱和”)溶液,若升温至40℃,形成的溶液质量为150g,则烧杯中溶液的溶质质量分数为33.3%(精确到0.1%)
③某温度时,氯化钠与硝酸钾的溶解度相等,则溶解度的最小取值范围是36g<S<36.6g.
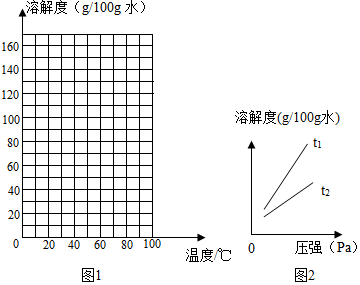
④根据表中数据,请在图1坐标图中描点、绘制符合KNO3溶解度变化规律的曲线如图.
⑤固体硝酸钾中混有少量氯化钠可以通过溶解、蒸发浓缩、降温结晶、过滤等步骤分离提纯硝酸钾.可以利
用该方法分离的理由是ⅠⅡ.
Ⅰ.固体混合物中硝酸钾的含量较高,氯化钠的含量较低
Ⅱ.硝酸钾的溶解度受温度影响变化较大
Ⅲ.40℃至100℃,硝酸钾的溶解度始终大于氯化钠
⑥气体的溶解度也有一定的变化规律.
不同温度下,氧气的溶解度随压强变化如图2所示,图中t2对应的温度为30℃,则t1对应的温度A.
A.小于30℃B.等于30℃C.大于30℃D.无法确定.
| 温度(℃) | 10 | 20 | 40 | 60 | 80 |
| KNO3 | 20.9 | 31.6 | 63.9 | 110 | 169 |
| NaCl | 35.8 | 36 | 36.6 | 37.3 | 38.4 |
②在20℃时,将50克硝酸钾溶解在100克水中,形成的是饱和(填“饱和”或“不饱和”)溶液,若升温至40℃,形成的溶液质量为150g,则烧杯中溶液的溶质质量分数为33.3%(精确到0.1%)
③某温度时,氯化钠与硝酸钾的溶解度相等,则溶解度的最小取值范围是36g<S<36.6g.
④根据表中数据,请在图1坐标图中描点、绘制符合KNO3溶解度变化规律的曲线如图.

⑤固体硝酸钾中混有少量氯化钠可以通过溶解、蒸发浓缩、降温结晶、过滤等步骤分离提纯硝酸钾.可以利
用该方法分离的理由是ⅠⅡ.
Ⅰ.固体混合物中硝酸钾的含量较高,氯化钠的含量较低
Ⅱ.硝酸钾的溶解度受温度影响变化较大
Ⅲ.40℃至100℃,硝酸钾的溶解度始终大于氯化钠
⑥气体的溶解度也有一定的变化规律.
不同温度下,氧气的溶解度随压强变化如图2所示,图中t2对应的温度为30℃,则t1对应的温度A.
A.小于30℃B.等于30℃C.大于30℃D.无法确定.
