题目内容
12.为了测定硫酸溶液中溶质的质量分数,取一定量的生铁样品5.8g放入100g硫酸溶液中恰好完全反应(杂质不参加反应),所得氢气的质量为0.2g.请 计算该硫酸溶液中溶质的质量分数(保留小数点后一位).分析 铁和稀硫酸反应生成硫酸亚铁和氢气,根据氢气的质量可以计算硫酸的质量,进一步可以计算该硫酸溶液中溶质的质量分数.
解答 解:设硫酸的质量为x,
Fe+H2SO4═FeSO4+H2↑,
98 2
x 0.2g
$\frac{98}{x}$=$\frac{2}{0.2g}$,
x=9.8g,
该硫酸溶液中溶质的质量分数为:$\frac{9.8g}{100g}$×100%=9.8%,
答:该硫酸溶液中溶质的质量分数为9.8%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
20.下列与水有关的说法正确的是( )
| A. | 澄清透明的液体就是水 | B. | 可用肥皂水区分硬水和软水 | ||
| C. | 用活性炭吸附可以降低水的硬度 | D. | 水结成冰是因为水分子发生变化 |
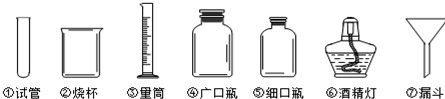
7.如图所示实验操作正确的是( )
| A. |  | B. |  | C. |  | D. |  |
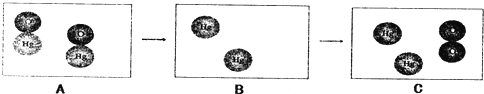
 表示碳原子,
表示碳原子, 表示氧原子,
表示氧原子, 表示氢原子.
表示氢原子.