题目内容
7.填写下列空白.(1)写出下列物质的化学式
烧碱NaOH;苏打Na2CO3;
(2)下列属于溶液的是BCE(填序号)
A.水 B.澄清石灰水 C.酒精 D.豆浆 E.碘酒.
分析 (1)根据化学式是元素符号和小数字组成的表示物质组成的式子.在化合物中正负化合价代数和为0,正价在前,负价在后进行分析;
(2)根据溶液是均一、稳定的混合物;溶液的本质特征是均一性、稳定性,属于混合物进行分析.
解答 解:(1)烧碱是氢氧化钠,在氢氧化钠中钠显示+1价,氢氧根离子显示-1价,化学式为:NaOH;
烧碱是碳酸钠,在碳酸钠中,钠元素显示+1价,碳酸根离子显示-2价,化学式为:Na2CO3;
(2)A、水是纯净物,不属于溶液;
B、澄清石灰水是均一稳定的混合物,属于溶液;
C、酒精是酒精的水溶液,是均一稳定的混合物,属于溶液;
D、豆浆属于胶体,不属于溶液;
E、碘酒是碘的酒精溶液,是均一稳定的混合物,属于溶液.
故选:BCE.
故答案为:(1)NaOH;Na2CO3;
(2)BCE.
点评 本题主要考查化学式的书写和意义,难度较小.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
18.甲、乙、丙、丁四位同学用锌和稀硫酸反应,所得相关数据记录如下:(误差忽略不计)
计算:
(1)甲同学加入的金属锌的质量x.
(2)稀硫酸中溶质的质量分数.
| 甲 | 乙 | 丙 | 丁 | |
| 取用的稀硫酸的质量/g | 100 | 100 | 100 | 100 |
| 加入金属的质量/g | x | 1.25x | 1.5x | 2x |
| 生成氢气的质量/g | 0.4 | 0.5 | 0.6 | 0.6 |
(1)甲同学加入的金属锌的质量x.
(2)稀硫酸中溶质的质量分数.
2.某合金样品为Fe-C合金、Fe-Zn合金和Fe-Al合金中的一种,为测定其组成,实验室只提供一瓶未标明质量分数的稀硫酸和必要的仪器.取出合金粉末5.6克与足量该硫酸充分反应,经测定,产生了气体a克.以下判断一定正确的是( )
| A. | 0.03<a<0.2 Fe-C合金 | B. | 0.17<a<0.2 Fe-Zn合金 | ||
| C. | a>0.2 Fe-C合金 | D. | 0.2<a<0.58 Fe-Al合金 |
16.下列物质在氧气中燃烧能产生明亮蓝紫色火焰的是( )
| A. | 木条 | B. | 硫 | C. | 铁 | D. | 磷 |
3.下列物质放入水中,能形成溶液的是( )
| A. | 面粉 | B. | 植物油 | C. | 食盐 | D. | 碳酸钙 |
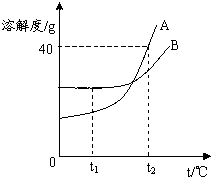 如图所示,A、B分别是两种固体物质的溶解度曲线.
如图所示,A、B分别是两种固体物质的溶解度曲线. 老师每次做有关镁的实验时都会强调:镁是一种银白色有金属光泽的金属.但拿出的镁条总是有一层灰黑色的“外衣”,这层灰黑色的外衣是什么物质呢?
老师每次做有关镁的实验时都会强调:镁是一种银白色有金属光泽的金属.但拿出的镁条总是有一层灰黑色的“外衣”,这层灰黑色的外衣是什么物质呢?