题目内容
碳酸钙是钙的碳酸盐化合物,工业用途甚广.
(1)石灰石用途非常广泛.可用来吸收火力发电厂煤燃烧时产生的二氧化硫废气,请将反应的化学方程式补充完整:2CaCO3+2SO2+O2 2CaSO4+______.
2CaSO4+______.
(2)电子工业高纯碳酸钙的制备.硝酸钙与碳酸铵在溶液中反应的化学方程式是:Ca(NO3)2+(NH4)2CO3=CaCO3↓+2NH4NO3,采用______操作进行沉淀分离.
(3)常用工业碳酸钙(含有少量NaCl、FeCl3等杂质)为原料生产某融雪剂.主要生产流程如图所示.已知:Fe(OH)3为难溶的碱.
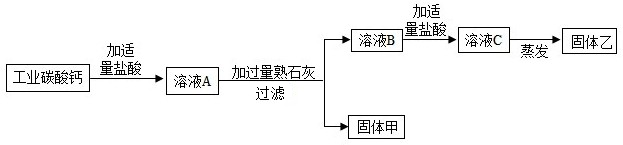
①碳酸钙与盐酸反应的化学方程式是______.
②溶液A加入过量熟石灰的主要目的是______.
③固体乙的成分是______.
解:(1)由反应的化学方程式2CaCO3+O2+2SO2═2CaSO4+X,根据化学变化前后原子的种类、数目不变,可判断生成物X的含有2个C原子和4个O原子,则每个分子由1个C原子和2个O原子构成,物质的化学式为CO2.
(2)产物碳酸钙难溶于水,硝酸铵易溶于水,因此可以采用过滤法分离;
(3)①碳酸钙与盐酸反应产生氯化钙、水和氧气,反应的方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
②碳酸钙经盐酸反应后的溶液A中含有少量Fe3+杂质,加入过量的氢氧化钙和氯化铁反应产生氢氧化铁沉淀,把杂质除去;
③由变化的流程可知固体C中含有原混合物中的氯化钠,和反应过程中生成的氯化钙;
故答案为:(1)2CO2 ;(2)过滤;
(3)①CaCO3+2HCl=CaCl2+H2O+CO2↑;②使FeCl3沉淀完全;③CaCl2、NaCl.
分析:(1)根据化学反应前后原子的种类和数目不变进行解答;
(2)根据难溶性的固体和液体分离采用过滤法;
(3)①碳酸钙与盐酸反应产生氯化钙、水和氧气,写出反应的方程式;
②根据碳酸钙中含有的杂质分析,加入过量氢氧化钙能把杂质离子沉淀出来;
③依据流程中物质反应的情况分析乙中存在的物质即可.
点评:此题是对与融雪相关的问题考查,涉及面广知识点较基础,质量守恒定律的运用、过滤分离混合物的原理、除杂的方法等,重点是强化基础知识的学习,能够考查同学们的综合分析能力.
(2)产物碳酸钙难溶于水,硝酸铵易溶于水,因此可以采用过滤法分离;
(3)①碳酸钙与盐酸反应产生氯化钙、水和氧气,反应的方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
②碳酸钙经盐酸反应后的溶液A中含有少量Fe3+杂质,加入过量的氢氧化钙和氯化铁反应产生氢氧化铁沉淀,把杂质除去;
③由变化的流程可知固体C中含有原混合物中的氯化钠,和反应过程中生成的氯化钙;
故答案为:(1)2CO2 ;(2)过滤;
(3)①CaCO3+2HCl=CaCl2+H2O+CO2↑;②使FeCl3沉淀完全;③CaCl2、NaCl.
分析:(1)根据化学反应前后原子的种类和数目不变进行解答;
(2)根据难溶性的固体和液体分离采用过滤法;
(3)①碳酸钙与盐酸反应产生氯化钙、水和氧气,写出反应的方程式;
②根据碳酸钙中含有的杂质分析,加入过量氢氧化钙能把杂质离子沉淀出来;
③依据流程中物质反应的情况分析乙中存在的物质即可.
点评:此题是对与融雪相关的问题考查,涉及面广知识点较基础,质量守恒定律的运用、过滤分离混合物的原理、除杂的方法等,重点是强化基础知识的学习,能够考查同学们的综合分析能力.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
氧化物、酸、碱、盐都是重要的无机化合物.请按要求回答下列一系列相关的问题.
(1)产生下列现象,只和空气中的水蒸气有关的是
A.固体烧碱要密封存放
B.生石灰长期在空气中放置会变质
C.浓硫酸露置于空气中会增重、变稀
D.铁制品放在潮湿空气中会生锈
(2)以下是一些食物的近似pH,对于胃酸过多的人比较适宜的食物是
(3)根据“性质决定用途,用途体现性质”回答下列问题.
A.稀释浓硫酸时,为什么不可将水倒进浓硫酸里?请简要解释其原因.
B.盐酸等许多酸都能使紫色石蕊试液变红,为什么?
C.写出用稀盐酸除水垢(主要成分是碳酸钙)的化学方程式.
(4)三支试管中分别装有少量白色固体,它们分别是氯化钠、氢氧化钠、碳酸钙中的一种,只要加入足量的 就能将它们一次性鉴别出来;盐酸(分析纯)化学式HCl质量分数36%密度l.18g/cm3
(5)实验操作考试时某同学做了如下两个实验:①氧化铜与稀硫酸反应;②烧碱溶液与酚酞溶液反应.实验结束后,该同学发现废液缸中有蓝色沉淀.请你写出有蓝色沉淀生成的反应的化学方程式是 .
(6)右图是浓盐酸试剂瓶上标签的部分内容.请回答:
A.现要配制9%的稀盐酸120g,需要这种浓盐酸 g;
B.浓盐酸使用一段时间后溶质质量分数变小的原因是什么?
C.某固体氢氧化钠在空气中敞口放置一段时间后部分变质,将该固体取10g加入质量分数为9%的盐酸至不再产生气泡为止,共产生气体质量为2.2g,试计算未变质的氢氧化钠的质量为多少克?
(1)产生下列现象,只和空气中的水蒸气有关的是
A.固体烧碱要密封存放
B.生石灰长期在空气中放置会变质
C.浓硫酸露置于空气中会增重、变稀
D.铁制品放在潮湿空气中会生锈
(2)以下是一些食物的近似pH,对于胃酸过多的人比较适宜的食物是
| 选项 | A | B | C | D |
| 物质 | 橘子 | 泡菜 | 葡萄 | 玉米粥 |
| pH | 2.9~3.5 | 3.0~4.0 | 3.5~4.5 | 6.8-8.0 |
A.稀释浓硫酸时,为什么不可将水倒进浓硫酸里?请简要解释其原因.
B.盐酸等许多酸都能使紫色石蕊试液变红,为什么?
C.写出用稀盐酸除水垢(主要成分是碳酸钙)的化学方程式.
(4)三支试管中分别装有少量白色固体,它们分别是氯化钠、氢氧化钠、碳酸钙中的一种,只要加入足量的
(5)实验操作考试时某同学做了如下两个实验:①氧化铜与稀硫酸反应;②烧碱溶液与酚酞溶液反应.实验结束后,该同学发现废液缸中有蓝色沉淀.请你写出有蓝色沉淀生成的反应的化学方程式是
(6)右图是浓盐酸试剂瓶上标签的部分内容.请回答:
A.现要配制9%的稀盐酸120g,需要这种浓盐酸
B.浓盐酸使用一段时间后溶质质量分数变小的原因是什么?
C.某固体氢氧化钠在空气中敞口放置一段时间后部分变质,将该固体取10g加入质量分数为9%的盐酸至不再产生气泡为止,共产生气体质量为2.2g,试计算未变质的氢氧化钠的质量为多少克?
 (2010?三明)2010年全国“两会”代表和委员们首次使用环保“石头纸”制作的便笺和文件袋.“石头纸”是一种低碳经济的绿色产品,它的主要成分是一种含钙的盐类化合物.某学习小组对“石头纸”进行如下图所示实验,观察到澄清石灰水变浑浊.
(2010?三明)2010年全国“两会”代表和委员们首次使用环保“石头纸”制作的便笺和文件袋.“石头纸”是一种低碳经济的绿色产品,它的主要成分是一种含钙的盐类化合物.某学习小组对“石头纸”进行如下图所示实验,观察到澄清石灰水变浑浊.
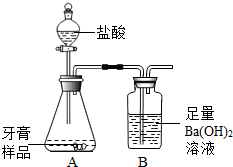 (2013?高邮市二模)化学兴趣小组对某品牌牙膏中碳酸钙含量进行以下探究.该牙膏摩擦剂主要由碳酸钙、氢氧化铝组成,其他成分遇到盐酸时无气体生成.现利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定B中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.请回答下列问题.
(2013?高邮市二模)化学兴趣小组对某品牌牙膏中碳酸钙含量进行以下探究.该牙膏摩擦剂主要由碳酸钙、氢氧化铝组成,其他成分遇到盐酸时无气体生成.现利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定B中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.请回答下列问题.