题目内容
8. 生活中我们经常见到由金属材料制成的日用品,请根据所学知识回答:
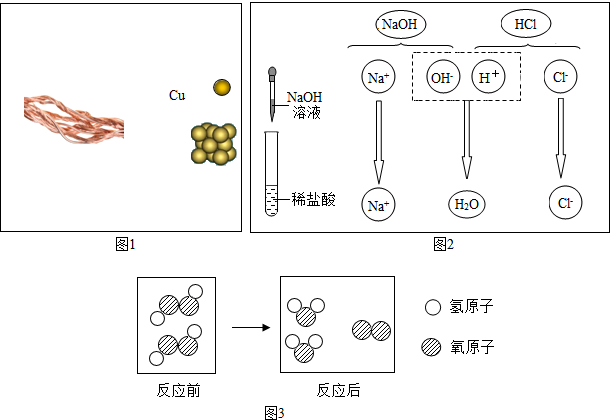
生活中我们经常见到由金属材料制成的日用品,请根据所学知识回答:(1)青少年一定要爱护自己的眼睛,在光线不足时看书、写字要用照明工具.右图是一种照明用台灯.
①如图中标示的各部件中,用金属材料制成的是①(填一种物质的序号).
②灯管后面的反光片为铝箔.铝块能制成铝箔是利用了铝的延展性.
③铝具有良好抗腐蚀性能的原因4Al+3O2=2Al2O3(写化学方程式)
(2)波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、生石灰加水配制而成.配制波尔多液不能用铁制容器?Fe+CuSO4=FeSO4+Cu(写化学方程式)
(3)图中涉及到了Fe、Cu、Al三种金属,可选用下列中的AB验证 Fe、Cu、Al 三种金属的活动性顺序,
A. CuSO4溶液、Fe、Al2(SO4)3溶液 B.Cu、Al、FeSO4 溶液
C.Fe、Al、CuSO4 溶液 D. Fe、Cu、H2SO4 溶液
(4)在氯化铜和氯化亚铁的混合溶液中加入一定质量的镁粉,充分反应后过滤,得到滤渣和滤液.
①滤液中一定含有的溶质是MgCl2(填化学式);
②向滤渣中滴加稀盐酸,有气泡产生,则滤渣中一定含有的物质是Cu、Fe(填化学式).
分析 根据物质的制成材料的类别、物质的性质进行分析解答,铁能与硫酸铜反应生成硫酸亚铁和铜;验证金属活动性顺序,可以依据两金夹一盐或是两盐夹一金的方法;在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,据此解答.
解答 解:(1)①如图中标示的各部件中,用金属材料制成的是铁螺丝钉、铝箔反光片、铜质插头,故填:①.
②铝块能制成铝箔是利用了铝的延展性,故填:延展.
③铝具有良好抗腐蚀性能是因为铝能被氧气氧化生成致密的氧化铝保护膜,故填:4Al+3O2=2Al2O3.
(2)配制波尔多液不能用铁制容器,因为硫酸铜能与铁反应生成硫酸亚铁和铜,故填:Fe+CuSO4=FeSO4+Cu.
(3)要Fe、Cu、Al 三种金属的活动性顺序,可以采用两金夹一盐或是两盐夹一金的方法;
A. CuSO4溶液、Fe、Al2(SO4)3溶液,是两盐夹一金的方法,铁能与硫酸铜反应,铁与硫酸铝不反应,故能证明Fe、Cu、Al 三种金属的活动性顺序,正确;
B.Cu、Al、FeSO4 溶液,是两金夹一盐的方法,铝能与硫酸亚铁反应,铜不与硫酸亚铁反应,故能证明Fe、Cu、Al 三种金属的活动性顺序,正确;
C.Fe、Al、CuSO4 溶液,铁和铝都能与硫酸铜溶液反应,说明铁和铝的活动性强于铜,不能说明铁和铝的活动性,错误;
D. Fe、Cu、H2SO4 溶液,只能证明铁的活动性强于铜,不能证明与铝的关系,错误;
故填:AB.
(4)在氯化铜和氯化亚铁的混合溶液中加入一定质量的镁粉,充分反应后过滤,得到滤渣和滤液.
①镁能与氯化铜反应生成氯化镁,故滤液中一定含有的溶质是MgCl2;故填:MgCl2;
②向滤渣中滴加稀盐酸,有气泡产生,说明含有氢前的金属,镁能与氯化亚铁反应生成铁,则滤渣中一定含有的物质是Cu、Fe,故填:Cu、Fe.
点评 本题考查的是金属的有关性质的应用,完成此题,可以依据金属的性质以及金属活动性顺序的意义进行.

 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案| A. | 2Na:“2”表示两个钠元素 | |
| B. | 2OH-:“2”表示两个氢氧根离子 | |
| C. | $\stackrel{+2}{Mg}$:“+2”表示镁元素的化合价为+2 | |
| D. | NO2:“2”表示一个二氧化氮分子含有一个氧分子 |
| A. | 镁条在空气中燃烧,发出耀眼的白光,放出热量,生成黑色粉末状固体 | |
| B. | 铁丝在氧气中剧烈燃烧,火星四射,放出热量,生成红色固体 | |
| C. | 木炭在氧气中燃烧,发出白光,放出热量,产生能使澄清石灰水变浑浊的气体 | |
| D. | 红磷在空气中燃烧,产生大量白雾,放出热量,生成白色固体 |
| 血浆 | 乳汁 | 唾液 | 胆汁 | 胰液 | 胃液 | |
| pH范围 | 7.3~7.45 | 6.6~7.6 | 6.6~7.1 | 7.1~7.3 | 7.5~8.0 | 0.9~1.5 |
| A. | 血浆 | B. | 胃液 | C. | 乳汁 | D. | 唾液 |
| A. | 打磨石器 | B. | 烧制陶瓷 | C. | 冶炼钢铁 | D. | 合成腈纶 |
| A. | 太阳能 | B. | 电能 | C. | 化学能 | D. | 风能 |