题目内容
2.向100g溶质质量分数为10%的氢氧化钾溶液中,加入100g溶质质量分数为10%的稀硫酸,充分反应后,向该溶液中加入紫色石蕊溶液,溶液颜色为( )| A. | 红色 | B. | 紫色 | C. | 蓝色 | D. | 无色 |
分析 根据题给的氢氧化钾溶液的氢氧化钾的质量和硫酸溶液中硫酸的质量,然后结合氢氧化钾和稀硫酸反应的化学方程式判断那种物质过量.
解答 解:氢氧化钾溶液的氢氧化钠的质量100g×10%=10g,100g溶质质量分数为10%的稀硫酸中溶质的质量100g×10%=10g;
2KOH+H2SO4═K2SO4+2H2O,
112 98
10g 10g
通过比较可以看出,氢氧化钾有剩余,向所得溶液中滴加石蕊溶液,则石蕊溶液变蓝.
答案:C
点评 本题主要考查学生运用化学方程式进行计算的能力.学生须认真分析题意,找出各物质间的关系,正确写出方程式,判断那种物质过量,才能正确解答.

练习册系列答案
相关题目
12.为了研究锌和铝与盐酸反应的不同,某研究小组进行了如下探究.
(1)小明设计的实验方案:向表面积相同的铝片和锌粒中分别加入盐酸.写出锌与盐酸反应的化学方程式:Zn+2HCl═ZnCl2+H2↑.
(2)小芳将去膜和未去膜的铝片分别放入盐酸中,发现前者比后者产生气泡快,原因是未去膜的铝片表面有氧化铝(氧化膜),氧化铝先与盐酸反应.
(3)小芳在(2)实验中,还观察到有“灰黑色沉淀”这一异常现象出现.
【提出问题】铝与盐酸反应出现的灰黑色沉淀的组成是什么?
【查阅文献】铝在颗粒较小时为灰黑色;AlCl3为无色透明晶体或白色而微带浅黄色的固体,易溶于水和乙醇.
【提出合理假设】假设a:该灰黑色沉淀可能含有铝(或铝和氯化铝的混合物);
假设b:该灰黑色沉淀可能含有AlCl3;
假设c:该灰黑色沉淀可能含有难溶于酸的物质.
【设计并完成实验】取灰黑色沉淀分别进行如表实验.
【得出结论】由实验①可判断假设c不成立(填“成立”或“不成立”),再结合②和③可得出该灰黑色沉淀的成分是铝和氯化铝.
(1)小明设计的实验方案:向表面积相同的铝片和锌粒中分别加入盐酸.写出锌与盐酸反应的化学方程式:Zn+2HCl═ZnCl2+H2↑.
(2)小芳将去膜和未去膜的铝片分别放入盐酸中,发现前者比后者产生气泡快,原因是未去膜的铝片表面有氧化铝(氧化膜),氧化铝先与盐酸反应.
(3)小芳在(2)实验中,还观察到有“灰黑色沉淀”这一异常现象出现.
【提出问题】铝与盐酸反应出现的灰黑色沉淀的组成是什么?
【查阅文献】铝在颗粒较小时为灰黑色;AlCl3为无色透明晶体或白色而微带浅黄色的固体,易溶于水和乙醇.
【提出合理假设】假设a:该灰黑色沉淀可能含有铝(或铝和氯化铝的混合物);
假设b:该灰黑色沉淀可能含有AlCl3;
假设c:该灰黑色沉淀可能含有难溶于酸的物质.
【设计并完成实验】取灰黑色沉淀分别进行如表实验.
| 实验编号 | 实验操作 | 实验现象 |
| ① | 加入适量稀盐酸 | 有微量气泡,固体全部溶解,得到澄清溶液 |
| ② | 加入适量蒸馏水 | 固体部分溶解 |
| ③ | 加入适量无水乙醇 | 固体部分溶解 |
13.下列因素与物质的溶解度大小无关的是( )
| A. | 溶质的性质 | B. | 溶剂的性质 | C. | 温度 | D. | 质量 |
10.(1)表是元素周期表的一部分,请你根据表回答问题:
①氧的相对原子质量是16.00.
②表中,金属元素有三种.13号元素的元素符号是Al.
(2)图甲是某元素在元素周期表中的部分信息,图乙是该元素的一种粒子结构示意图.
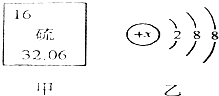
①该元素的原子的核电荷数为16,相对原子质量为32.06.
②图乙所示粒子的符号为S2-.
| 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
| 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13? 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 29.95 |
②表中,金属元素有三种.13号元素的元素符号是Al.
(2)图甲是某元素在元素周期表中的部分信息,图乙是该元素的一种粒子结构示意图.

①该元素的原子的核电荷数为16,相对原子质量为32.06.
②图乙所示粒子的符号为S2-.
17.下列关于分子和原子的叙述中,正确的是( )
| A. | 分子质量大于原子的质量 | |
| B. | 分子能运动而原子不能运动 | |
| C. | 分子受热体积变大,遇冷体积变小 | |
| D. | 在化学反应中分子可分而原子不可分 |
14.蜡烛燃烧生成二氧化碳和水.下列关于该化学反应的叙述正确的是( )
| A. | 燃烧前后蜡烛的质量没有改变 | |
| B. | 蜡烛减少的质量等于生成的二氧化碳和水的质量 | |
| C. | 蜡烛燃烧后生成物的质量之和等于蜡烛减少的质量与消耗氧气的质量之和 | |
| D. | 燃烧前蜡烛的质量与消耗氧气质量之和等于生成的二氧化碳与水的质量之和 |
 小明发现他的铜制眼镜框上出现一些绿色的锈渍,他决定到实验室在老师的帮助下对该成分进行探究.
小明发现他的铜制眼镜框上出现一些绿色的锈渍,他决定到实验室在老师的帮助下对该成分进行探究.