题目内容
黄铜是铜和锌的合金(Cu-Zn),可用来制造电器零件及日用品。为测定某黄铜样品中铜的质量分数(不考虑黄铜中其他杂质),当向10g黄铜样品粉末中加入98g稀硫酸时恰好完全反应,称得烧杯中物质的质量为107.9g。请计算:
(1)反应生成氢气的质量为_________g。
(2)此黄铜样品中铜的质量分数。
(1)反应生成氢气的质量为_________g。
(2)此黄铜样品中铜的质量分数。
(1)0.1
(2)解:设样品中Zn的质量为x。
Zn+H2SO4==ZnSO4+H2↑
65 2
x 0.1g
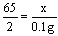 ;
;
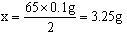
铜的质量分数为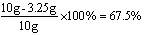
答:黄铜样品中铜的质量分数为67.5%。
(2)解:设样品中Zn的质量为x。
Zn+H2SO4==ZnSO4+H2↑
65 2
x 0.1g
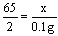 ;
;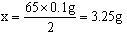
铜的质量分数为
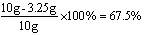
答:黄铜样品中铜的质量分数为67.5%。

练习册系列答案
相关题目