题目内容
4.某金属混合物是由镁和X二种金属组成,取2.4克混合物,与100克一定溶质质量分数的稀硫酸恰恰好完全反应,得到W克氢气,则下列说法正确的是( )| A. | 如果X是锌,则W不可能是0.18克 | |
| B. | 如果X是铜,且W等于0.1克,则铜和镁的质量相等 | |
| C. | 如果X是铁,则溶液可能为浅绿色且质量仍可能等于100克 | |
| D. | 如果X是铝,则稀硫酸的溶质质量分数不大于9.8% |
分析 假设这2.4 g全部为镁,根据金属与酸反应时生成氢气的质量=$\frac{金属元素的化合价}{金属的相对原子质量}×金属的质量$,可计算出生成氢气为0.2g,可以推知等质量的Zn、Al、Fe产生氢气的质量,由此得出混合金属与酸反应产生氢气的质量范围,据此分析判断有关的说法.
解答 解:假设2.4g全部为镁,与稀硫酸恰好反应生成氢气质量为:$\frac{2}{24}×2.4g$=0.2g
同理可计算出2.4g的锌、铁、铝与稀硫酸反应产生氢气的质量分别是:0.07g、0.09g、0.27g;铜与酸反应不产生氢气.
A、如果X是锌,镁锌的混合金属与酸反应产生的氢气的质量应在0.07g到0.2g之间,则W可能是0.18克,故A错误;
B、如果X是铜,且W等于0.1克,由于铜与酸不反应,产生的氢气由镁产生,则可计算出镁的质量是1.2g,则铜的质量是2.4g-1.2g=1.2g,则铜和镁的质量相等,故B正确;
C、如果X是铁,则溶液为浅绿色,由于金属与酸反应溶液的质量增大,溶液的质量不可能等于100克,故C错误;
D、2.4g镁消耗硫酸的质量为9.8g,即此时硫酸的浓度为9.8%,但是等质量的铝消耗硫酸的质量更多,所以若混合物为Al、Mg,则稀硫酸中溶质质量分数一定大于9.8%,故D错误.
故选:B.
点评 相同质量的金属与酸反应产生氢气的质量的多少与金属的相对原子质量和化合价有关.同价态的金属若相对原子质量越大,产生的氢气质量越小.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.对下列生活中的现象或做法解释不合理的是( )
| 选项 | 现象或做法 | 解释 |
| A | 湿衣服在阳光下比在阴凉处更易晾干 | 温度越高,分子运动越快 |
| B | 油锅着火用锅盖盖灭 | 使可燃物与空气隔绝 |
| C | 铝制品比铁制品更耐腐蚀 | 铝表面易形成致密氧化膜 |
| D | 用洗洁精去餐盘上的油渍 | 洗洁精能溶解油渍 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
15.以下是我们日常生活中常用的清洗剂,其名称及有效成分如下表:
(1)“洁厕灵”可以清除铁锈(主要成分是氧化铁),写出该反应的化学方程式Fe2O3+6HCl═2FeCl3+3H2O.
(2)“洁厕灵”与“84”消毒液混合会发生如下反应:2HCl+NaClO═X+H2O+Cl2↑,对人体造成伤害.下列说法不正确的是②(填序号).
①物质X由离子构成
②NaClO中氯元素的化合价为-1
③“洁厕灵”能用于清除水垢(主要成分是碳酸钙和氢氧化镁)
④对人体造成伤害的物质是氯气
(3)“污渍爆炸盐”溶于水,生成Na2CO3和H2O2,再加入足量的“洁厕灵”,产生能使澄清石灰水变浑浊的气体,写出产生该气体的化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑.
(4)“活氧彩漂”可用于漂洗衣物、杀菌消毒等,原因是其有效成分过氧化氢分子中含有“过氧基”(-O-O-).据此推测,下列物质中可用作杀菌消毒剂的是D(填序号).
| 清洗剂的名称 | 洁厕灵 | “84”消毒液 | 污渍爆炸盐 | 活氧彩漂 |
| 有效成分 | 盐酸 | NaClO | 过碳酸钠 | 过氧化氢 |
(2)“洁厕灵”与“84”消毒液混合会发生如下反应:2HCl+NaClO═X+H2O+Cl2↑,对人体造成伤害.下列说法不正确的是②(填序号).
①物质X由离子构成
②NaClO中氯元素的化合价为-1
③“洁厕灵”能用于清除水垢(主要成分是碳酸钙和氢氧化镁)
④对人体造成伤害的物质是氯气
(3)“污渍爆炸盐”溶于水,生成Na2CO3和H2O2,再加入足量的“洁厕灵”,产生能使澄清石灰水变浑浊的气体,写出产生该气体的化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑.
(4)“活氧彩漂”可用于漂洗衣物、杀菌消毒等,原因是其有效成分过氧化氢分子中含有“过氧基”(-O-O-).据此推测,下列物质中可用作杀菌消毒剂的是D(填序号).
| 选 项 | A | B | C | D |
| 物质的名称 | 水 | 乙酸 | 二氧化碳 | 过氧乙酸 |
| 物质的结构式 | 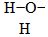 | 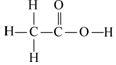 | O=C=O | 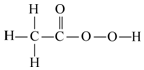 |
19.生活中常见的下列物质,不属于溶液的是( )
| A. | 糖水 | B. | 牛奶 | C. | 白酒 | D. | 汽水 |
16.在CuO和Zn的混合物中加入一定质量的稀盐酸,微热,待反应停止后过滤,滤除不溶物后再向滤液中加入一枚铁钉,若铁钉无变化,则下列叙述不正确的是( )
| A. | 不溶物中一定含有铜 | |
| B. | 滤液全部是氯化锌溶液 | |
| C. | 向滤液中滴加硝酸银溶液,一定有白色沉淀产生 | |
| D. | 向不溶物中滴加稀盐酸,一定有气泡产生 |
14.向一定量的AgNO3和Cu(NO3)2的混合溶液中加入一定量的锌粉,充分反应后过滤,得到滤液M和滤渣N;向滤液M中加入稀盐酸,有白色沉淀生成.下列分析判断的说法中,正确的是( )
| A. | 滤液M中一定存在Cu2+ | |
| B. | 滤渣N中一定存在Ag、Cu | |
| C. | 滤液M的质量大于原混合溶液的质量 | |
| D. | 滤渣N的质量小于加入锌粉的质量 |
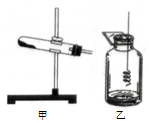 实验安全很重要,小柯在实验室制取并收集了一瓶氧气,并用来做铁丝在氧气中燃烧的实验.
实验安全很重要,小柯在实验室制取并收集了一瓶氧气,并用来做铁丝在氧气中燃烧的实验.