题目内容
12.人类的生活和生产都离不开金属材料.(1)在汽车电路中,经常用铜作导线,这是利用了铜的导电性.
(2)铁生锈的条件是:铁与空气中的水、氧气直接接触,根据铁生锈的条件,自行车支架大梁采取的防锈措施是喷漆.
(3)用赤铁矿(主要成分Fe2O3)为原料,炼铁的主要反应的化学方程式是Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,在这一反应中,铁元素的化合价由+3价变为0价.
(4)波尔多液是果树生产上经常使用的一种农药,它是用胆矾|生石灰和水混合制得的,在配制波尔多液时不能用铁制容器配制,原因是Fe+CuSO4═FeSO4+Cu(用化学方程式表示).
(5)某同学为了验证镁、铜、银的活动性顺序,他选择了打磨过的铜丝,你认为他还需要的另外两种溶液是硫酸镁溶液和硝酸银溶液,请根据选定的试剂写出上述实验中发生反应的一个化学方程式Cu+2AgNO3=Cu(NO3)2+2Ag.
分析 (1)根据金属的性质与用途来分析;
(2)根据铁生锈的条件分析,铁与空气和水同时接触.根据防止金属生锈的方法通常是把金属和空气或水隔绝分析;
(3)根据工业炼铁的原理找出反应物、生成物以及反应条件书写方程式,根据反应前后元素的化合价进行分析;
(4)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可;
(5)根据金属活动性顺序的验证方法进行分析.
解答 解:(1)用铜作导线,这是利用了铜的导电性;故填:导电;
(2)铁生锈的条件是铁与空气中的氧气和水同时接触;常见的自行车它的支架采用的防锈措施是喷漆;故填:水、氧气;喷漆;
(3)一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;反应物中的氧化铁中的铁显+3价,生成物中的铁是单质,显0价,故答案为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;+3;0;
(4)铁和硫酸铜溶液反应生成硫酸亚铁和铜,不能用铁制的容器配制波尔多液,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu;故填:Fe+CuSO4═FeSO4+Cu;
(5)在金属活动性顺序中,镁>铜>银,可以采用两边夹中间的方法选择试剂,铜是单质,则镁和银选用其盐溶液进行,故可以选用硫酸镁溶液和硝酸银溶液,铜能与硝酸银反应生成硝酸铜和银.故填:硫酸镁;硝酸银;Cu+2AgNO3=Cu(NO3)2+2Ag.
点评 本题考查常见金属的性质,金属生锈的条件,金属活动性大小的验证方法,化学方程式的书写等,要牢固掌握.

练习册系列答案
相关题目
3.如图表示治理汽车尾气所涉及反应的微观过程,下列说法不正确的是( )


| A. | 图中所示单质的化学式为N2 | |
| B. | 反应后分子个数变少了 | |
| C. | 生成物中单质与化合物的质量比为7:11 | |
| D. | 该反应使有害气体转化为无害气体 |
20.下列物质常用于改良酸性土壤的是( )
| A. | 石灰石 | B. | 烧碱 | C. | 食盐 | D. | 熟石灰 |
4.鉴别下列各组物质的方法中不能达到目的是( )
| A. | 用肥皂水,可区分硬水和软水 | |
| B. | 用相互刻画的方法,可以比较硬铝和铝的硬度 | |
| C. | 用水,可鉴别氯化钠和氢氧化钠两种固体 | |
| D. | 点燃根据火焰的颜色,可区分一氧化碳和氢气 |
1.氮元素能形成多种氧化物,下列氧化物中氮元素的化合价为+4的是( )
| A. | NO | B. | NO2 | C. | N2O | D. | N2O5 |
8. 人类的生产和生活都离不开金属.
人类的生产和生活都离不开金属.
(1)铁是应用最广泛的金属.工业常用磁铁矿和一氧化碳在高温条件下炼铁,该反应的化学方程式为Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2.
(2)下表是一些金属熔点的数据.
保险丝由铋、铅、锡、镉等金属组成,其熔点约为B.
A.20-40℃B.60-80℃C.230-250℃D.300-320℃
(3)向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法不正确的是AC
A.a点对应溶液中的溶质有2种
B.c点对应溶液中溶质为Zn(NO3)2
C.b~c段对应溶液中一定含有AgNO3
D.取d点对应固体,加入稀盐酸,有气泡产生.
 人类的生产和生活都离不开金属.
人类的生产和生活都离不开金属.(1)铁是应用最广泛的金属.工业常用磁铁矿和一氧化碳在高温条件下炼铁,该反应的化学方程式为Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2.
(2)下表是一些金属熔点的数据.
| 金属 | 铜 | 锌 | 锡 | 铅 | 铋 | 镉 |
| 熔点/℃ | 1083 | 419.6 | 231.9 | 327.5 | 271.3 | 320.9 |
A.20-40℃B.60-80℃C.230-250℃D.300-320℃
(3)向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法不正确的是AC
A.a点对应溶液中的溶质有2种
B.c点对应溶液中溶质为Zn(NO3)2
C.b~c段对应溶液中一定含有AgNO3
D.取d点对应固体,加入稀盐酸,有气泡产生.
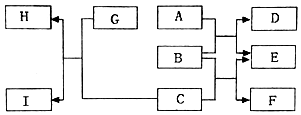 A-I表示初中化学常见的物质,其中,C的浓溶液常用作干燥某些气体,H是最清洁燃料,D是蓝色沉淀,各物质间相互转化关系如图所示,请回答下列问题:
A-I表示初中化学常见的物质,其中,C的浓溶液常用作干燥某些气体,H是最清洁燃料,D是蓝色沉淀,各物质间相互转化关系如图所示,请回答下列问题: