题目内容
某有机物的相对分子质量为46,4.6g该物质在氧气中充分燃烧生成8.8g二氧化碳和5.4g水,据此判断,该有机物( )A.只由碳、氢两种元素组成
B.一定含有碳、氢、氧三种元素
C.化学式为CH2O2
D.分子中C、Η、O原子个数比为2:6:1
【答案】分析:根据元素守恒可判断物质中一定含有C和H两种元素,对氧元素的确定要根据二氧化碳与氧气中氧元素的质量来分析.
解答:解:一种物质燃烧只生成水和二氧化碳,则该物质肯定含有碳和氢元素.是否含氧则可根据质量守恒定律由下法确定:
8.8g二氧化碳中含氧元素的质量为:8.8g× =6.4g,含碳元素的质量为:8.8g-6.4g=2.4g;
=6.4g,含碳元素的质量为:8.8g-6.4g=2.4g;
5.4g水中含氧元素的质量为:5.4g× =4.8g,含氢元素的质量为:5.4g-4.8g=0.6g;
=4.8g,含氢元素的质量为:5.4g-4.8g=0.6g;
则4.6g某纯净物中含氧的质量为::4.6g-2.4g-0.6g=1.6g;
某纯净物中原子个数比为C:H:O=(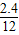 :
: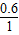 :
: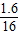 )=2:6:1;
)=2:6:1;
所以该物质的化学是为:C2H6O.
故选:BD.
点评:本题较好的考查了学生的分析计算能力和对元素守恒以及质量守恒的运用,属于很典型的习题,但对氧元素的确定及含量容易出错.
解答:解:一种物质燃烧只生成水和二氧化碳,则该物质肯定含有碳和氢元素.是否含氧则可根据质量守恒定律由下法确定:
8.8g二氧化碳中含氧元素的质量为:8.8g×
 =6.4g,含碳元素的质量为:8.8g-6.4g=2.4g;
=6.4g,含碳元素的质量为:8.8g-6.4g=2.4g;5.4g水中含氧元素的质量为:5.4g×
 =4.8g,含氢元素的质量为:5.4g-4.8g=0.6g;
=4.8g,含氢元素的质量为:5.4g-4.8g=0.6g;则4.6g某纯净物中含氧的质量为::4.6g-2.4g-0.6g=1.6g;
某纯净物中原子个数比为C:H:O=(
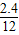 :
: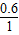 :
: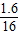 )=2:6:1;
)=2:6:1;所以该物质的化学是为:C2H6O.
故选:BD.
点评:本题较好的考查了学生的分析计算能力和对元素守恒以及质量守恒的运用,属于很典型的习题,但对氧元素的确定及含量容易出错.

练习册系列答案
相关题目
某有机物的相对分子质量为46,4.6g该物质在氧气中充分燃烧生成8.8g二氧化碳和5.4g水,据此判断,该有机物( )
| A、只由碳、氢两种元素组成 | B、一定含有碳、氢、氧三种元素 | C、化学式为CH2O2 | D、分子中C、Η、O原子个数比为2:6:1 |