题目内容
5.暖宝宝(如图1所示)是一种防寒用品,某小组探究暖宝宝中的主要成分有哪些?
【提出问题】暖宝宝中的主要成分是什么?
【初步实验】剪开内包装袋,倒出其中的粉末,发现呈黑色.用磁铁吸引,黑色粉末部分被吸引
【查阅资料】
1、常见黑色粉末是炭粉、铁粉、二氧化锰、氧化 铜、四氧化三铁
2、四氧化三铁具有磁性,能被磁铁吸引
【提出猜想】黑色粉末中可能含有铁粉、四氧化三铁粉末或两者都有
【进行实验】取黑色粉末放入燃烧匙中点燃,伸入盛有氧气的集气瓶中(瓶底放入少量澄清石灰水),在瓶内剧烈燃烧,火星四射,放出大量热,生成黑色固体;实验后,盖上玻璃片振荡集气瓶,发现变浑浊.
【得出结论】该黑色粉末一定含有铁粉和碳粉.写出铁粉燃烧的文字表达式铁+氧气$\stackrel{点燃}{→}$四氧化三铁;
【实验反思】此实验中澄清石灰水除了用于证明二氧化碳是否存在间接确定黑色粉末是否含有炭粉外,还具有的作用是防止铁粉反应后的熔化物溅落瓶底使集气瓶底炸裂.
【实验延伸】查阅资料暖宝宝中除了上述物质外,还有蛭石、氯化钠和少量水,发热原理是利用铁生锈:铁与氧气、水反应生成氢氧化亚铁.粉末中氯化钠、活性炭会加速生锈.利用暖宝宝证明空气中氧气含量,装置如图2:
| 测定 项目 | 实验前 | 实验后 | |
| 烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)的体积 | |
| 体积/mL | 80 | 42 | 200 |
(2)上述装置中会有少量水残留在导管中造成实验误差,请你用以下实验用品对上述实验加以改进.(量筒、大烧杯、玻璃棒、水、暖宝宝),在图3框中画出实验装置示意图即可.
分析 【进行实验】考虑铁粉在氧气中燃烧的现象,从而证明了铁粉的存在.考虑二氧化碳的鉴别方法.
【得出结论】铁粉燃烧生成四氧化三铁;
【实验反思】根据铁丝燃烧现象分析;
【实验延伸】根据实验数据分析,改用量筒进行实验.
解答 解:【进行实验】取适量黑色粉末于燃烧匙中,在酒精灯上点燃后伸入盛有氧气的集气瓶中,观察到剧烈燃烧、火星四射、放出大量热、生成黑色固体的现象,从而证明了铁粉的存在.在反应后的集气瓶中加入澄清的石灰水振荡,因为二氧化碳使澄清石灰水变浑浊,故观察到石灰水变浑浊,说明粉末中一定含有碳粉;
【得出结论】铁与氧气反应的文字表达式:铁+氧气$\stackrel{点燃}{→}$四氧化三铁.
【实验反思】在反应后的集气瓶中加入澄清的石灰水振荡,因为二氧化碳使澄清石灰水变浑浊,故观察到石灰水变浑浊,说明粉末中一定含有碳粉;同时防止铁粉反应后的熔化物溅落瓶底使集气瓶底炸裂.
【实验延伸】空气中氧气含量为$\frac{80mL-42mL}{200mL}$×100%=19%;
由于上述装置中会有少量水残留在导管中造成实验误差,可以去掉导管,改用量筒进行实验,如图
故答案为:【进行实验】生成黑色固体; 变浑浊
【得出结论】铁+氧气$\stackrel{点燃}{→}$四氧化三铁;
【实验反思】防止铁粉反应后的熔化物溅落瓶底使集气瓶底炸裂;
【实验延伸】19; .
.
点评 该题为综合实验题,考查的知识点较多,氧气的性质,装置气密性的检验等,关键是熟记相关知识点.语言表述要简练准确.掌握铁的化学性质,空气中氧气含量的测定.

练习册系列答案
相关题目
15.解决“白色污染”问题,下列做法不宜提倡的是( )
| A. | 减少塑料制品 | B. | 重复使用某些塑料制品 | ||
| C. | 使用新型可降解塑料 | D. | 焚烧废弃塑料 |
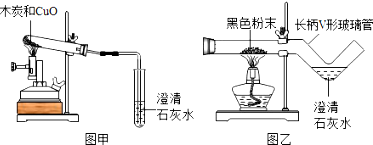
16.我国劳动人民早在五千年前就会使用木炭炼铜.在化学实验室里模拟炼铜,既可用传统的实验装置(见图甲),又能用改进的微型实验装置(见图乙).化学兴趣小组采用图乙装置,开展以下探究活动.
【提出问题】木炭与CuO反应所得红色固体中含有什么物质?
【查阅资料】
(1)写出木炭与CuO反应的化学方程式:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑,若该反应进行的不彻底,产物中还有氧化亚铜(Cu2O,红色固体).
(2)Cu不溶于稀硫酸,Cu2O能与稀硫酸反应得到蓝色CuSO4溶液:Cu2O+H2SO4═Cu+CuSO4+H2O.
【作出猜想】红色固体的成分:①全部是Cu;②全部是Cu2O;③既有Cu也有Cu2O.
【实验探究】
(1)取木炭、CuO两种黑色粉末适量,再加少许CaC12(能降低反应温度,加快反应速率)均匀混合,然后将黑色粉末装入长柄V形玻璃管的直管内.
(2)按图乙连好实验装置,然后加热反应物;2分钟后,黑色粉末出现红热现象,同时澄清的石灰水变浑浊,此时停止加热.
(3)待玻璃管冷却后,提取里面的红色固体,进行如下的验证:(相对原子质量Cu-64 O-16)
【评价反思】
(1)使用图乙装置与使用图甲装置相比,其优点是节约药品(写出1条即可).
(2)若要证明CaC12是该反应的催化剂,还需要验证CaCl2的质量和化学性质在反应前后不变.

【提出问题】木炭与CuO反应所得红色固体中含有什么物质?
【查阅资料】
(1)写出木炭与CuO反应的化学方程式:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑,若该反应进行的不彻底,产物中还有氧化亚铜(Cu2O,红色固体).
(2)Cu不溶于稀硫酸,Cu2O能与稀硫酸反应得到蓝色CuSO4溶液:Cu2O+H2SO4═Cu+CuSO4+H2O.
【作出猜想】红色固体的成分:①全部是Cu;②全部是Cu2O;③既有Cu也有Cu2O.
【实验探究】
(1)取木炭、CuO两种黑色粉末适量,再加少许CaC12(能降低反应温度,加快反应速率)均匀混合,然后将黑色粉末装入长柄V形玻璃管的直管内.
(2)按图乙连好实验装置,然后加热反应物;2分钟后,黑色粉末出现红热现象,同时澄清的石灰水变浑浊,此时停止加热.
(3)待玻璃管冷却后,提取里面的红色固体,进行如下的验证:(相对原子质量Cu-64 O-16)
| 步骤 | 现象 | 结论 |
| ①取1.44g红色固体装入试管,滴入足量的稀硫酸,充分反应 | 红色固体部分减少,溶液变 为蓝色 | 猜想①错误 |
| ②滤出试管中残留的红色固体,洗涤干燥,称其质量为1.04g | 猜想③正确 |
(1)使用图乙装置与使用图甲装置相比,其优点是节约药品(写出1条即可).
(2)若要证明CaC12是该反应的催化剂,还需要验证CaCl2的质量和化学性质在反应前后不变.
20.下列由事实得出的结论正确的是( )
| 编号 | 事实 | 结论 |
| A | 某气体不能使带火星木条复燃 | 该气体一定不含氧气 |
| B | 某物质可以与氧气发生反应 | 该反应一定属于氧化反应 |
| C | 某元素的粒子最外层电子数为8 | 该粒子一定是稀有气体的原子 |
| D | 某物质组成中只含有一种元素 | 该物质一定是单质 |
| A. | A | B. | B | C. | C | D. | D |
10.下列各项中,成因果关系的是( )
①大气中二氧化碳增加 ②二氧化硫、二氧化氮排入大气中
③冰箱致冷剂氟利昂等排入大气中 ④一氧化碳大量排入空气中
a形成酸雨 b产生温室效应 c破坏臭氧层 d 使人中毒.
①大气中二氧化碳增加 ②二氧化硫、二氧化氮排入大气中
③冰箱致冷剂氟利昂等排入大气中 ④一氧化碳大量排入空气中
a形成酸雨 b产生温室效应 c破坏臭氧层 d 使人中毒.
| A. | ①---d | B. | ②---a | C. | ③---b | D. | ④---c |
17.下列实验现象叙述正确的是( )
| A. | 木炭在氧气中燃烧,生成二氧化碳气体 | |
| B. | 硫在氧气中燃烧发出微弱的淡蓝色火焰 | |
| C. | 红磷在空气中燃烧产生大量白烟 | |
| D. | 铁丝在空气中剧烈燃烧,火星四射,生成黑色固体 |
