题目内容
11.某化学兴趣小组进行了“配制70g20%的氯化钠溶液”的实验.该实验的部分操作如图所示.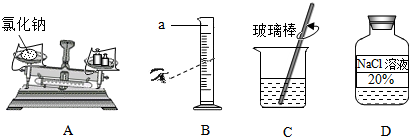
(1)配制此氯化钠溶液的步骤为:计算、称量、溶解、装瓶;其中B(填序号)的操作是错误的操作;
(2)需要称取氯化钠的质量是14g;
(3)20%的意义是每100份质量的氯化钠溶液中含有20份质量的氯化钠.
分析 (1)根据配制溶质质量分数一定的溶液的基本步骤,结合量筒读数时视线要与凹液面的最低处保持水平,进行分析解答.
(2)利用溶质质量=溶液质量×溶质的质量分数,进行分析解答.
(3)根据溶质质量分数的含义进行分析解答.
解答 解:(1)配制70g20%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解、装瓶;量取液体时,视线与液体的凹液面最低处保持水平,图中仰视刻度,操作错误.
(2)溶质质量=溶液质量×溶质的质量分数,配制70g20%的氯化钠溶液,需要称取氯化钠的质量是70g×20%=14g.
(3)20%的意义是每100份质量的氯化钠溶液中含有20份质量的氯化钠.
故答案为:(1)计算;称量;B;(2)14;(3)每100份质量的氯化钠溶液中含有20份质量的氯化钠.
点评 本题难度不大,掌握配制溶质质量分数一定的溶液的基本步骤、量筒的使用方法等是正确解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.如图为某化学反应的微观示意图,图中“●”表示硫原子,“○”表示氧原子.下列说法中错误的是( )


| A. | 甲是SO2 | |
| B. | 该反应属于化合反应 | |
| C. | 反应前后,原子种类、原子数目均不变 | |
| D. | 反应中,甲、乙、丙三种物质的分子个数比为1:1:1 |
16.以下物质由原子直接构成的是( )
| A. | 氧气 | B. | 二氧化碳 | C. | 氮气 | D. | 铜 |
3.生活中的下列现象,用分子的相关知识解释,不正确的是( )
| A. | 水受热变成水蒸气,说明水分子分裂变成了原子 | |
| B. | 经过花园,闻到鲜花的香味,说明分子在不断运动 | |
| C. | 氧气经加压后可以贮存在钢罐中,说明分子间有间隙 | |
| D. | 氢气可燃而氧气却能助燃,说明分子种类不同化学性质不同 |
20.下列问题的研究中,未利用对比实验思想方法的是( )
| A. |  研究空气中氧气含量 | B. |  研究微粒的运动 | ||
| C. |  研究木炭在氧气中燃烧 | D. |  研究分子运动快慢与温度关系 |
 “新盖中盖”高钙片的标签如右,且知此钙片成分中只有碳酸钙含有钙元素.请仔细阅读后回答下列问题:
“新盖中盖”高钙片的标签如右,且知此钙片成分中只有碳酸钙含有钙元素.请仔细阅读后回答下列问题: