题目内容
1.现有下列实验装置,请回答下列问题: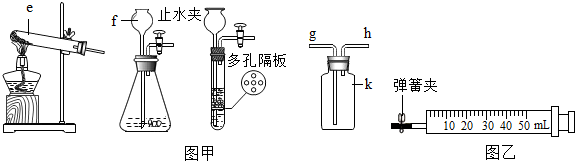
(1)图中e、f仪器的名称:e试管,f长颈漏斗,k集气瓶.
(2)用氯酸钾和二氧化锰制氧气,选用发生装置A(填字母A、B、C、D),反应符号表达式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.反应基本类型为分解反应.
(3)关闭B装置中的止水夹后,从长颈漏斗向锥形瓶中注入一定量的水,静止一段时间后如图所示,则B装置不漏气(填“漏气”、“不漏气”或“无法确定”).
(4)常温下用块状固体和液体反应制气体时,改用C装置(多孔隔板用来放块状固体)代替B装置的优点是AC(选填下列说法的序号).A.可以随时加液 B.可以控制反应速率 C.可以控制反应发生与停止
观察图C装置,制气体反应处于进行(填“进行”或“停止”)中.
(5)实验室用双氧水和二氧化锰粉末制氧气的符号表达式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,该实验若选用C装置不能(填“能”或“不能”)达到(4)中所说优点.若用D装置来收集生成的氧气,气体应从g(填g或h)通入.某同学将带火星的木条伸入到收集满氧气的集气瓶内,木条复燃,拿出木条,盖好集气瓶.过一会儿,再用带火星的木条伸人瓶内,木条仍然复燃.重复几次后,木条不再复燃.据此现象你能得到的结论是带火星的木条是否复燃与氧气的浓度有关.
(6)测定空气中氧气含量:使用如图装置进行实验.实验原理是利用脱氧剂中铁单质在常温下消耗装置内氧气(脱氧剂在空气中放置一段时间,有红棕色固体生成).实验前应先进行的操作是检验装置气密性.
【实验过程】
步骤1:在注射器中放入足量脱氧剂粉末,封闭;
步骤2:打开弹簧夹,将活塞向右拉至一定距离,关闭弹簧夹;
步骤3:不断轻轻晃动注射器,至活塞位置不再发生变化.
【数据处理】
①实验中需要记录的数据有AB(填字母).
A.反应前注射器中原有空气的体积 B.反应后注射器中剩余气体的体积
②上述实验测定过程至少需要重复两次,其目的是减少实验误差,最终计算得出氧气约占空气的体积分数.
【实验评价】
①放入的脱氧剂足量的目的是将氧气完全耗尽.
②与燃烧红磷法相比,脱氧剂法测定空气中氧气含量的优点是没有有毒物质散逸到空气中,环保.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据实验室用氯酸钾和二氧化锰制取氧气的反应物是固体,反应条件是加热,氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气进行分析;
(3)根据检验B装置气密性的正确操作进行分析;
(4)根据C装置的特点进行分析;
(5)根据过氧化氢在二氧化锰的催化作用下生成水和氧气,二氧化锰是粉末状,氧气密度比空气大,化学反应的现象与反应物的浓度有关进行分析;
(6)根据有气体参加的反应,组装好仪器要首先检验装置的气密性进行分析;
【数据处理】
①根据实验中需要记录的数据是:注射器原来的空气的体积、反应后注射器活塞进入后显示剩余气体的体积进行分析;
②根据上述实验测定过程至少需要重复两次,其目的是:使测量的结果更准确进行分析;
【实验评价】
①根据实验成功的关键是:装置要严密,红磷要足量进行分析;
②根据脱氧剂法测定空气中氧气含量的优点是:不受氧气含量多少的影响,使结果更准确,以及脱氧剂生成物是红色氧化铁固体等进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,a是酒精灯,f是长颈漏斗,g是集气瓶;
(2)实验室用氯酸钾和二氧化锰制取氧气的反应物是固体,反应条件是加热,所以发生装置是:A,氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,该反应满足分解反应一变多的条件,属于分解反应;
(3)通过分析可知,检验B装置气密性的正确操作是:关闭B装置中的止水夹后,从长颈漏斗向锥形瓶中注入一定量的水,静止一段时间后形成一段稳定的水柱,证明装置气密性良好;
(4)常温下用块状固体和液体反应制气体时,改用C装置(多孔隔板用来放块状固体)代替B装置的优点是:长颈漏斗可以添加液体,利用压强和重力作用可以控制反应的发生和停止,故选:AC,观察图C装置,固体和液体接触,制气体反应处于进行中;
(5)过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,二氧化锰是粉末状,所以该实验若选用C装置不能达到(4)中所说优点,氧气密度比空气大,所以用D装置来收集生成的氧气,气体应从g通入,化学反应的现象与反应物的浓度有关,所以能得到的结论是:带火星的木条是否复燃与氧气的浓度有关;
(6)有气体参加的反应,组装好仪器要首先检验装置的气密性,所以使用图2装置进行实验,实验前应先进行的操作是:检查装置的气密性;
【数据处理】
①实验中需要记录的数据是:注射器原来的空气的体积、反应后注射器活塞进入后显示剩余气体的体积,故选:AB;
②上述实验测定过程至少需要重复两次,其目的是:使测量的结果更准确,减小实验误差;
【实验评价】
①实验成功的关键是:装置要严密,红磷要足量;
②脱氧剂法测定空气中氧气含量的优点是:不受氧气含量多少的影响,使结果更准确,以及脱氧剂生成物是红色氧化铁固体等.
故答案为:(1)试管,长颈漏斗,集气瓶;
(2)A,2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,分解;
(3)不漏气;
(4)AC,进行;
(5)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,不能,g,带火星的木条是否复燃与氧气的浓度有关;
(6)检查装置的气密性,AB,减少实验误差,将氧气完全耗尽;没有有毒物质散逸到空气中,环保.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案| A. | 碳元素的质量之比为1:1 | B. | 氧原子的个数之比为1:2 | ||
| C. | CO和CO2的分子个数之比为11:7 | D. | 氧元素的质量之比为14:11 |
| A. |  火箭发射 | B. |  节日焰火 | C. |  风力发电 | D. |  葡萄酿酒 |
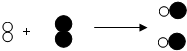 在光照或点燃条件下,氢气和氯气发生反应生成氯化氢,其反应的微观示意图如下:下列说法正确的是( )
在光照或点燃条件下,氢气和氯气发生反应生成氯化氢,其反应的微观示意图如下:下列说法正确的是( )| A. | 化学反应在反应前后分子个数可能不发生变化 | |
| B. | 此反应过程中只有物质变化,没有能量变化 | |
| C. | 在任何条件下,H2和Cl2一定不能大量共存 | |
| D. | 该反应是化合反应 |
| A. | 原子的质量主要集中在原子核上,但是原子核的体积很小 | |
| B. | 原子是构成物质的最小微粒 | |
| C. | 元素是以原子中的质子数来分类的 | |
| D. | 在化学变化中分子分成原子,原子种类则没有发生改变 |
| A. | +3 | B. | -5 | C. | -3 | D. | +5 |
 如图为某药厂生产的“新盖中盖牌”高钙片标签上的部分文字,请仔细阅读后回答下列问题.
如图为某药厂生产的“新盖中盖牌”高钙片标签上的部分文字,请仔细阅读后回答下列问题.