题目内容
除去下列括号中的杂质,写出化学方程式:HCl(H2SO4) ;FeSO4(CuSO4) .
考点:物质除杂或净化的探究,酸的化学性质,盐的化学性质
专题:物质的分离、除杂、提纯与共存问题
分析:根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答:解:要除去HCl中的H2SO4,实质就是除去硫酸根离子,可利用H2SO4与氯化钡溶液反应生成硫酸钡沉淀和盐酸,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:H2SO4+BaCl2=BaSO4↓+2HCl.
要除去FeSO4溶液中的CuSO4,实质就是除去铜离子,可利用铁粉与硫酸铜溶液应生成硫酸亚铁和铜,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Fe+CuSO4=Cu+FeSO4.
故答案为:H2SO4+BaCl2=BaSO4↓+2HCl;Fe+CuSO4=Cu+FeSO4.
要除去FeSO4溶液中的CuSO4,实质就是除去铜离子,可利用铁粉与硫酸铜溶液应生成硫酸亚铁和铜,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Fe+CuSO4=Cu+FeSO4.
故答案为:H2SO4+BaCl2=BaSO4↓+2HCl;Fe+CuSO4=Cu+FeSO4.
点评:物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列汉沽民间制作,其中属于化学变化的是( )
| A、民间绣十字绣 |
| B、版画厂木刻 |
| C、盐场晒盐 |
| D、玫瑰香葡萄酒 |
某同学用pH试纸测定溶液的酸碱度,下列操作或结论正确的是( )
| A、用pH试纸直接沾取待测溶液 |
| B、先用水润湿pH试纸再测定溶液酸碱度 |
| C、用pH试纸测得石灰水的pH=5 |
| D、用pH试纸测得盐酸的pH=1 |

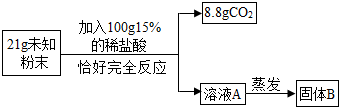
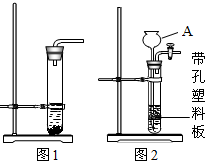 实验室常用石灰石与稀盐酸制取C02,某同学设计了两种制取CO2的部分装置(如图).
实验室常用石灰石与稀盐酸制取C02,某同学设计了两种制取CO2的部分装置(如图).