题目内容
18.如图是用等质量的Mg和Fe与足量的稀硫酸反应产生氢气的质量随反应时间的变化关系曲线,其中正确的是( )| A. |  | B. |  | C. |  | D. |  |
分析 由题意:质量相等的Mg和Fe与足量且质量分数相等的稀硫酸反应,根据Mg~H2SO4~H2↑,Fe~H2SO4~H2↑,Mg产生氢气的质量比Fe产生氢气的质量多,同时Mg消耗的硫酸质量也比Fe消耗的硫酸质量多.因为两种金属的活动性不相同,所以它们反应所需的时间也不相同.
解答 解:
将等质量的Mg和Fe投入到足量稀H2SO4中,则铁和镁全部参加反应,
Mg+H2SO4═MgSO4+H2↑
24 2
Fe+H2SO4═FeSO4+H2↑
56 2
通过反应的化学方程式以及金属与酸反应生成氢气的质量关系可以看出,镁生成的氢气大于铁.
Mg的金属活动性比Fe强,故Mg用的时间少.
故选A.
点评 本题考查了常见物质的性质及物质间的反应,完成此题,可以依据已有的知识结合图象进行.解答这类题的关键是,读懂图象本意,审清图象内涵.准确理解并应用图象中的相关信息,正确解题.

练习册系列答案
相关题目
6.符合以下四位同不所描述的化学式可能是( )
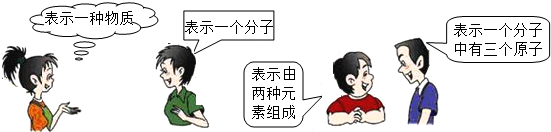

| A. | CO2 | B. | O2 | C. | MgO | D. | HClO |
10.推理是一种重要的学习方法.下列推理中正确的是( )
| A. | 氧化物中一定含有氧元素,则含氧元素的化合物一定是氧化物 | |
| B. | 分子发生改变的变化一定是化学变化,则化学变化中分子一定发生改变 | |
| C. | 单质是由一种元素组成的物质,则由一种元素组成的物质一定是单质 | |
| D. | 离子是带电荷的微粒,则带电荷的微粒一定是离子 |
8.下列有关化学知识的说法正确的是( )
| A. | 所有原子的原子核都是由质子和中子构成 | |
| B. | 凡是含有氧元素的化合物都是氧化物 | |
| C. | 塑料属于合成材料 | |
| D. | 可燃物只要达到着火点就能燃烧 |
 如图是水分子在通电条件下分解的示意图.从图中你可以获得哪些信息,请任写三条:
如图是水分子在通电条件下分解的示意图.从图中你可以获得哪些信息,请任写三条: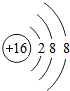 表示的粒子S2-.
表示的粒子S2-.