题目内容
11.要除去以下四种物质中的少量杂货,可选用的试剂及操作方法如下表,正确的( )| 选项 | 物质 | 杂质 | 可选用的试剂及操作方法 |
| A | NaCl | Na2CO3 | 溶解,加适量的盐酸,搅拌,蒸发 |
| B | KOH | K2CO3 | 溶解,加过量的石灰水,过滤,蒸发 |
| C | KCl | MnO2 | 溶解、过滤、蒸发结晶 |
| D | CaCO3 | KNO3 | 加适量的盐酸,蒸发 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、溶解后,Na2CO3能与适量的盐酸反应生成氯化钠、水和二氧化碳,再搅拌,蒸发,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
B、K2CO3能与过量的石灰水反应生成碳酸钙沉淀和氢氧化钾,能除去杂质但引入了新的杂质氢氧化钙(过量的),不符合除杂原则,故选项所采取的方法错误.
C、氯化钾易溶于水,二氧化锰难溶于水,可采取加水溶解、过滤、蒸发结晶的方法进行分离除杂,故选项所采取的方法正确.
D、CaCO3能与适量的盐酸反应生成氯化钙、水和二氧化碳,硝酸钾不与稀盐酸反应,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
故选:AC.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案
相关题目
5.氧化还原反应不一定有氧的得失,凡有元素化合价升降的反应都是氧化还原反应,下列反应中不属于四种基本反应类型但属于氧化还原反应的是( )
| A. | 2Na+2H2O═2NaOH+H2↑ | B. | CaC2+2H2O═Ca(OH)2+C2H2↑ | ||
| C. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | D. | CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O |
6.实验操作不当常引起误差.下列误差分析错误的是( )
| A. | 配制氯化钠溶液,称量时把砝码和氯化钠固体放反了,所得溶液溶质质量分数一定偏小 | |
| B. | 配制氢氧化钠溶液,所用固体已潮解,配得溶液溶质质量分数偏小 | |
| C. | 粗盐提纯,过滤时滤纸破损,则产率偏高 | |
| D. | 粗盐提纯,蒸发结晶时有固体飞溅,则产率偏低 |
3.下列物质的用途不仅仅是由它的化学性质决定的是( )
| A. | 盐酸用于除铁锈 | B. | 二氧化碳灭火 | ||
| C. | 天然气做燃料 | D. | 小苏打用于治疗胃酸过多 |
20.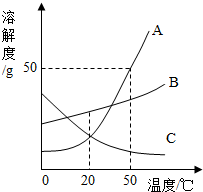 如图所示为A、B、C三种物质的溶解度曲线,下列分析不正确的是( )
如图所示为A、B、C三种物质的溶解度曲线,下列分析不正确的是( )
 如图所示为A、B、C三种物质的溶解度曲线,下列分析不正确的是( )
如图所示为A、B、C三种物质的溶解度曲线,下列分析不正确的是( )| A. | 20℃时,A、B、C三种物质的溶解度由大到小的顺序是B<A=C | |
| B. | 50℃时,把50gA放人50g水中能得到A的饱和溶液 | |
| C. | 将C的饱和溶液变为不饱和溶液,可采用降温的方法 | |
| D. | 将50℃时A、B、C三种物质的饱和溶液降温到20℃时,所得溶液的溶质质量分数的大小关系是B>C=A |
1.做空气中氧气含量测定的实验装置如图.下列有关说法正确的是( )
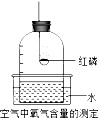

| A. | 选用红磷是因为反应可以耗尽O2,生成液态的五氧化二磷 | |
| B. | 燃烧匙中的红磷越多,水位上升越高 | |
| C. | 燃烧匙中的红磷可以换成铁丝 | |
| D. | 钟罩内气体压强的减小会导致水面的上升 |

