题目内容
15. 电镀厂的废水中含有Cu(NO3)2和AgNO3,为处理水体污染并回收金属,某兴趣小组的同学进行下列实验(如图所示):向含有Cu(NO3)2和AgNO3的废水中加入一定量的铁粉,过滤,得固体A和滤液B,向固体A中滴加稀盐酸,无明显现象,小组同学对所得滤液B的成分进行探究.
电镀厂的废水中含有Cu(NO3)2和AgNO3,为处理水体污染并回收金属,某兴趣小组的同学进行下列实验(如图所示):向含有Cu(NO3)2和AgNO3的废水中加入一定量的铁粉,过滤,得固体A和滤液B,向固体A中滴加稀盐酸,无明显现象,小组同学对所得滤液B的成分进行探究.【提出问题】过滤后所得滤液B中含有哪些成分?
【猜想与假设】
甲同学:滤液B中只含有Fe(NO3)2;
乙同学:滤液B中只含有Fe(NO3)2和AgNO3两种溶质;
丙同学:滤液B中只含有AgNO3和Cu(NO3)2两种溶质;
【表达与交流】写出甲同学猜想的理由:(1)加入的铁粉和溶液中的硝酸铜、硝酸银恰好完全反应,生成可溶的硝酸亚铁;
【反思与评价】请对乙同学的猜想做出评价:(2)不正确,这是因为铁粉先与硝酸银反应,后与硝酸铜反应,若滤液B中含有硝酸银,则滤液B中一定含有硝酸铜;
【实验探究】取滤液少许于试管中,向滤液中插入一根铜丝,看到铜丝表面有固体生成,则滤液B中溶质的化学式应该是(3)Fe (NO3)2、Cu(NO3)2、AgNO3;
【归纳总结】通过上述实验探究可知,在分析金属与盐溶液反应后的溶质成分时,需考虑的方面有(4)(至少答两方面)金属活动性顺序、反应物是否过量.
分析 铁比铜活泼,铜比银活泼,向含有Cu(NO3)2和AgNO3的废水中加入一定量的铁粉时,铁先和硝酸银反应,当硝酸银完全反应后,如果铁有剩余,则铁再和硝酸铜反应;
铁能和稀盐酸反应生成氯化亚铁和氢气;
铜能和硝酸银反应生成硝酸铜和银.
解答 解:【表达与交流】
如果铁粉和溶液中的硝酸铜、硝酸银恰好完全反应,则滤液B中只含有硝酸亚铁,因此甲同学猜想的理由是:加入的铁粉和溶液中的硝酸铜、硝酸银恰好完全反应,生成可溶的硝酸亚铁.
故填:加入的铁粉和溶液中的硝酸铜、硝酸银恰好完全反应,生成可溶的硝酸亚铁.
【反思与评价】
乙同学的猜想不正确,这是因为铁粉先与硝酸银反应,后与硝酸铜反应,若滤液B中含有硝酸银,则滤液B中一定含有硝酸铜.
故填:不正确,这是因为铁粉先与硝酸银反应,后与硝酸铜反应,若滤液B中含有硝酸银,则滤液B中一定含有硝酸铜.
【实验探究】
取滤液少许于试管中,向滤液中插入一根铜丝,看到铜丝表面有固体生成,说明滤液中含有硝酸银,进一步说明硝酸铜没有反应,因此滤液B中含有的溶质有铁和硝酸银反应生成的硝酸亚铁、没有反应的硝酸银和没有反应的硝酸铜,硝酸亚铁、硝酸铜和硝酸银的化学式是Fe (NO3)2、Cu(NO3)2、AgNO3.
故填:Fe (NO3)2、Cu(NO3)2、AgNO3.
【归纳总结】
通过上述实验探究可知,在分析金属与盐溶液反应后的溶质成分时,需考虑的方面有:金属活动性顺序、反应物是否过量等.
故填:;.金属活动性顺序;反应物是否过量.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
9.下列有关溶液的说法正确的是( )
| A. | 将植物油与水混合,得到的是溶液 | |
| B. | 配制溶液时,搅拌溶液可以增大溶质的溶解度 | |
| C. | 将10%的KNO3溶液倒出一半,剩余溶液中溶质的质量分数为20% | |
| D. | 饱和溶液在一定条件下可转化为不饱和溶液 |
6.下列实验操作中,正确的是( )
| A. | 给试管里的液体加热.液体体积不超过试管容积的$\frac{2}{3}$ | |
| B. | 将实验剩余的药品及时放回原试剂瓶 | |
| C. | 用酒精灯给试管内物质加热,试管的底部与灯芯接触 | |
| D. | 将颗粒状石灰石装入试管时,让石灰石缓缓地沿试管内壁滑到底部 |
10.在氯酸钾里加入少量的高锰酸钾,加热制氧的速率大大加快,其主要原因是( )
| A. | 高锰酸钾起了催化作用 | |
| B. | 高锰酸钾受热分解,使产生的氧气量大大增加 | |
| C. | 高锰酸钾受热分解生成的二氧化锰成为氯酸钾分解的催化剂 | |
| D. | 高锰酸钾比氯酸钾容易分解 |
20.下列不属于化学研究对象的是( )
| A. | 空气的组成 | B. | 潮汐现象 | C. | 氧气的性质 | D. | 水分子的构成 |
7. 同学们观察了如图所示的实验后,通过认真思考和积极讨论,得出了如下结论,你认为其中不合理的是( )
同学们观察了如图所示的实验后,通过认真思考和积极讨论,得出了如下结论,你认为其中不合理的是( )
 同学们观察了如图所示的实验后,通过认真思考和积极讨论,得出了如下结论,你认为其中不合理的是( )
同学们观察了如图所示的实验后,通过认真思考和积极讨论,得出了如下结论,你认为其中不合理的是( )| A. | 空气中含有能支持红磷燃烧的物质 | |
| B. | 红磷燃烧时产生白烟,说明生成了固体小颗粒 | |
| C. | 红磷燃烧后,钟罩内的物质都不溶于水 | |
| D. | 这个实验证明了氧气占空气总体积的$\frac{1}{5}$ |
4.下列为了达到实验目的而进行的实验操作,其中正确的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 洗涤内壁沾有油脂的试管 | 用大量的水冲洗 |
| B | 检验集气瓶中O2是否集满 | 将燃着的木条伸入集气瓶 |
| C | 检测CO中是否混有CO2 | 将气体通入澄清石灰水 |
| D | 除去KCl粉末中混有的K2SO4 | 加水溶解,过滤,蒸发结晶 |
| A. | A | B. | B | C. | C | D. | D |
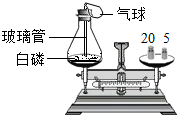 为了研究质量守恒定律,设计了如图“白磷燃烧前后质量测定”的实验,请分析有关问题:
为了研究质量守恒定律,设计了如图“白磷燃烧前后质量测定”的实验,请分析有关问题: