题目内容
某研究性学习小组的同学在一次探究活动中,对一份纯碱样品(含少量氯化钠)的纯度进行测定,请你参与并完成有关问题.
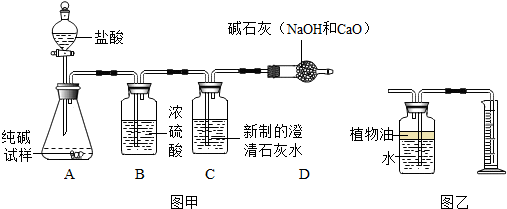
(1)甲同学进行如下操作:
①组装好如图甲仪器,并检查 ;
②称取6.0g试样放入锥形瓶中,加入少量蒸馏水溶解,并在其它装置中加入相应的药品;
③称量盛有新制澄清石灰水的装置C的质量;
④打开分液漏斗旋塞滴入盐酸,直到不再产生气泡为止;
⑤再次称量装置C的总质量产;
⑥计算出样品中碳酸钠的质量分数.
(2)图甲B装置的作用是 ;A装置中反应的化学方程式为: .
【意外发现】C瓶中石灰水没有变浑浊,同学们感到惊奇并产生了探究欲望.
【提出猜想】原因猜想:①是生成的气体中混有盐酸挥发出来的HCl;②是生成的气体流速太快,与石灰水反应产生了可溶性物质[经查资料分析可溶性物质是Ca(HCO3)2,它能与酸反应生成CO2等物质]
【实验探究]甲同学取少量实验后C瓶溶液于试管中,向其中依次滴加足量的稀HNO3和AgNO3溶液,无气泡但有沉淀产生.据此判断只有猜想 (填“①”或“②”)成立.
【交流讨论】对于如何改进实验,乙同学认为:应将盐酸换成稀硫酸、新制的澄清石灰水换成足量的NaOH溶液;丙同学认为:应在装置A和B之间插入一个盛有饱和NaHCO3溶液的洗气装置以吸收HCl(CO2不溶于饱和NaHCO3溶液,也不与其反应),并将新制的澄清石灰水换成足量的NaOH溶液.大家讨论后认为:乙同学的方案可行而丙同学的方案不可行.
【请你评价】丙同学方案不可行的原因是 .
【教师点拨】即便换成稀硫酸和氢氧化钠溶液,反应前后装置中存在的CO2也会使测定出的样品纯度不准确.
【请你改进】在上述基础上,你的措施是 .
同学们仍称取6.0g试样,用改进完善后的方案重新实验.
【数据处理]装置C实验前后两次称量的质量差为2.2g,则样品的纯度为 (计算结果有百分数表示,
保留到小数点后一位数字).
【实验反思】
①盛有NaOH溶液的洗气瓶还可换成盛有 的干燥管来吸收入CO2;
②若将C、D装置换成如图乙装置进行实验,也可达到预期实验目的,但要计算样品纯度时,除读取气体的体积数据外,还需要补充的数据是 ,图中植物油的作用为 ;
③若不用上述装置,而用生成沉淀的方法来测定试样中纯碱的质量分数,可选用的试剂是 .

(1)甲同学进行如下操作:
①组装好如图甲仪器,并检查
②称取6.0g试样放入锥形瓶中,加入少量蒸馏水溶解,并在其它装置中加入相应的药品;
③称量盛有新制澄清石灰水的装置C的质量;
④打开分液漏斗旋塞滴入盐酸,直到不再产生气泡为止;
⑤再次称量装置C的总质量产;
⑥计算出样品中碳酸钠的质量分数.
(2)图甲B装置的作用是
【意外发现】C瓶中石灰水没有变浑浊,同学们感到惊奇并产生了探究欲望.
【提出猜想】原因猜想:①是生成的气体中混有盐酸挥发出来的HCl;②是生成的气体流速太快,与石灰水反应产生了可溶性物质[经查资料分析可溶性物质是Ca(HCO3)2,它能与酸反应生成CO2等物质]
【实验探究]甲同学取少量实验后C瓶溶液于试管中,向其中依次滴加足量的稀HNO3和AgNO3溶液,无气泡但有沉淀产生.据此判断只有猜想
【交流讨论】对于如何改进实验,乙同学认为:应将盐酸换成稀硫酸、新制的澄清石灰水换成足量的NaOH溶液;丙同学认为:应在装置A和B之间插入一个盛有饱和NaHCO3溶液的洗气装置以吸收HCl(CO2不溶于饱和NaHCO3溶液,也不与其反应),并将新制的澄清石灰水换成足量的NaOH溶液.大家讨论后认为:乙同学的方案可行而丙同学的方案不可行.
【请你评价】丙同学方案不可行的原因是
【教师点拨】即便换成稀硫酸和氢氧化钠溶液,反应前后装置中存在的CO2也会使测定出的样品纯度不准确.
【请你改进】在上述基础上,你的措施是
同学们仍称取6.0g试样,用改进完善后的方案重新实验.
【数据处理]装置C实验前后两次称量的质量差为2.2g,则样品的纯度为
保留到小数点后一位数字).
【实验反思】
①盛有NaOH溶液的洗气瓶还可换成盛有
②若将C、D装置换成如图乙装置进行实验,也可达到预期实验目的,但要计算样品纯度时,除读取气体的体积数据外,还需要补充的数据是
③若不用上述装置,而用生成沉淀的方法来测定试样中纯碱的质量分数,可选用的试剂是
考点:实验探究物质的组成成分以及含量,常见气体的检验与除杂方法,盐的化学性质,书写化学方程式、文字表达式、电离方程式,根据化学反应方程式的计算
专题:科学探究
分析:(1)根据实验制取气体首先要装置的气密性进行解答;
(2)根据浓硫酸具有吸水性进行解答;碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳;
【实验探究】根据滴加足量稀HNO3和AgNO3溶液,无气泡但有沉淀产生,说明有氯化银生成,从而证明溶液中有氯离子存在进行解答;
【请你评价】根据NaHCO3饱和溶液吸收HCl时产生CO2,导致盛有NaOH溶液的洗气瓶质量增重偏大,造成误差进行解答;
【请你改进】根据原来装置内空气中存有二氧化碳气体,而使得计算结果不准确进行解答;
【数据处理】根据装置C实验前后两次称量的质量差为二氧化碳的质量可以求出碳酸钠的质量从而求出样品的纯度进行解答;
【实验反思】根据碳酸钠和氯化钡或氯化钙反应生成碳酸钡沉淀或碳酸钙沉淀而不和氯化钠反应进行解答.
(2)根据浓硫酸具有吸水性进行解答;碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳;
【实验探究】根据滴加足量稀HNO3和AgNO3溶液,无气泡但有沉淀产生,说明有氯化银生成,从而证明溶液中有氯离子存在进行解答;
【请你评价】根据NaHCO3饱和溶液吸收HCl时产生CO2,导致盛有NaOH溶液的洗气瓶质量增重偏大,造成误差进行解答;
【请你改进】根据原来装置内空气中存有二氧化碳气体,而使得计算结果不准确进行解答;
【数据处理】根据装置C实验前后两次称量的质量差为二氧化碳的质量可以求出碳酸钠的质量从而求出样品的纯度进行解答;
【实验反思】根据碳酸钠和氯化钡或氯化钙反应生成碳酸钡沉淀或碳酸钙沉淀而不和氯化钠反应进行解答.
解答:解:(1)实验制取气体首先要装置的气密性,所以组装好如图仪器,并检查装置的气密性;
(2)浓硫酸具有吸水性,图B装置的作用是干燥CO2气体;碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳;
【实验探究】滴加足量稀HNO3和AgNO3溶液,无气泡但有沉淀产生,说明有氯化银生成,从而证明溶液中有氯离子存在,说明生成的气体中混有盐酸挥发出来的HCl和碳酸钙反应生成氯化钙,所以①成立;
【请你评价】NaHCO3饱和溶液吸收HCl时产生CO2,导致盛有NaOH溶液的洗气瓶质量增重偏大,造成误差,所以丙同学方案不可行;
【请你改进】原来装置内空气中存有二氧化碳气体,而使得计算结果不准确,改进措施:两次称量前,均向整套装置中鼓入经NaOH溶液洗涤过的空气,目的是排尽装置中原有空气和反应后残留的CO2,且称量时C装置两端及B装置的出口封闭;
【数据处理】装置C实验前后两次称量的质量差为二氧化碳的质量,设碳酸钠的质量为x.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 2.2g
=
,解得x=5.3g
样品中碳酸钠的质量分数=
×100%=88.3%
答:样品的纯度为88.3%.
【实验反思】①盛有NaOH溶液的洗气瓶还可换成盛有碱石灰的干燥管来吸收入CO2;
②乙装置进行实验,除读取气体的体积数据外,还需要补充的数据是CO2在此状态下的密度,这样才能计算出质量,图中植物油的作用为防止部分CO2溶解在水中;
③碳酸钠和氯化钡或氯化钙反应生成碳酸钡沉淀或碳酸钙沉淀而不和氯化钠反应,若不用上述方法,而用生成沉淀的方法来测定试样中纯碱的质量分数,可选用的试剂是BaCl2或CaCl2溶液.
故答案为:(1)装置的气密性;(2)干燥CO2气体;Na2CO3+2HCl=2NaCl+H2O+CO2↑;【实验探究】①;
【请你评价】NaHCO3饱和溶液吸收HCl时产生CO2,导致盛有NaOH溶液的洗气瓶质量增重偏大,造成误差;
【请你改进】两次称量前,均向整套装置中鼓入经NaOH溶液洗涤过的空气,目的是排尽装置中原有空气和反应后残留的CO2,且称量时C装置两端及B装置的出口封闭;【数据处理】88.3%;【实验反思】①碱石灰;②CO2在此状态下的密度;防止部分CO2溶解在水中;③BaCl2(或CaCl2等).
(2)浓硫酸具有吸水性,图B装置的作用是干燥CO2气体;碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳;
【实验探究】滴加足量稀HNO3和AgNO3溶液,无气泡但有沉淀产生,说明有氯化银生成,从而证明溶液中有氯离子存在,说明生成的气体中混有盐酸挥发出来的HCl和碳酸钙反应生成氯化钙,所以①成立;
【请你评价】NaHCO3饱和溶液吸收HCl时产生CO2,导致盛有NaOH溶液的洗气瓶质量增重偏大,造成误差,所以丙同学方案不可行;
【请你改进】原来装置内空气中存有二氧化碳气体,而使得计算结果不准确,改进措施:两次称量前,均向整套装置中鼓入经NaOH溶液洗涤过的空气,目的是排尽装置中原有空气和反应后残留的CO2,且称量时C装置两端及B装置的出口封闭;
【数据处理】装置C实验前后两次称量的质量差为二氧化碳的质量,设碳酸钠的质量为x.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 2.2g
| 106 |
| x |
| 44 |
| 2.2g |
样品中碳酸钠的质量分数=
| 5.3g |
| 6.0g |
答:样品的纯度为88.3%.
【实验反思】①盛有NaOH溶液的洗气瓶还可换成盛有碱石灰的干燥管来吸收入CO2;
②乙装置进行实验,除读取气体的体积数据外,还需要补充的数据是CO2在此状态下的密度,这样才能计算出质量,图中植物油的作用为防止部分CO2溶解在水中;
③碳酸钠和氯化钡或氯化钙反应生成碳酸钡沉淀或碳酸钙沉淀而不和氯化钠反应,若不用上述方法,而用生成沉淀的方法来测定试样中纯碱的质量分数,可选用的试剂是BaCl2或CaCl2溶液.
故答案为:(1)装置的气密性;(2)干燥CO2气体;Na2CO3+2HCl=2NaCl+H2O+CO2↑;【实验探究】①;
【请你评价】NaHCO3饱和溶液吸收HCl时产生CO2,导致盛有NaOH溶液的洗气瓶质量增重偏大,造成误差;
【请你改进】两次称量前,均向整套装置中鼓入经NaOH溶液洗涤过的空气,目的是排尽装置中原有空气和反应后残留的CO2,且称量时C装置两端及B装置的出口封闭;【数据处理】88.3%;【实验反思】①碱石灰;②CO2在此状态下的密度;防止部分CO2溶解在水中;③BaCl2(或CaCl2等).
点评:此题是一道实验探究综合题,充分的展示了化学知识的方方面面,该题综合性强难度较大,对训练学生良好地思维品质以及知识的严密性有较好的帮助.

练习册系列答案
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案
相关题目
下列各组生活现象中,一定含有化学变化的是( )
| A、活性炭除臭 |
| B、樟脑球升华 |
| C、积雪化成水 |
| D、铁栅栏生锈 |
以下关于铁的叙述,错误的是( )
| A、生铁和钢都是铁元素的单质 |
| B、铁是电和热的导体 |
| C、铁制品在潮湿的空气中会生锈 |
| D、铁丝能在氧气中燃烧 |
下列物质在通常情况下不属于导体的是( )
| A、空气 胶木 |
| B、铜丝 人体 |
| C、烧碱溶液 石墨棒 |
| D、稀硫酸 食盐水 |
1998年春节前后,我国山西的假酒事件造成多人中毒死亡,其原因是( )
| A、假酒中含有甲醇 |
| B、假酒中乙醇含量过高 |
| C、假酒中含有碳酸 |
| D、假酒中含有醋酸 |
下列混合液中滴入Ba(OH)2溶液,立即产生白色沉淀的是( )
| A、Mg(NO3)2 HCl NaCl |
| B、CuCl2 NH4NO3 KCl |
| C、AlCl3 HNO3 CaCl2 |
| D、Na2CO3 KOH NaNO3 |
 如图是实验过滤装置图:
如图是实验过滤装置图: