题目内容
8.下列物质在一定条件下可以转化,请你用化学方程式表示下面转化的化学反应,并写出基本反应类型(反应基本类型填“化合”或“分解”)CO$\stackrel{①}{←}$C$\stackrel{②}{→}$ CO2 $\stackrel{③}{←}$CaCO3
①2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO、化合反应;
②C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2、化合反应;
③CaCO3+2HCl=CaCl2+H2O+CO2↑、复分解反应.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写;再根据反应特征确定反应类型.
解答 解:①碳不充分燃烧生成一氧化碳,反应的化学方程式为:2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO;该反应符合“多变一”的特征,属于化合反应.
②碳充分燃烧生成二氧化碳,反应的化学方程式为:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;该反应符合“多变一”的特征,属于化合反应.
③碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应.
故答案为:①2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO;化合反应;
②C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;化合反应;
③CaCO3+2HCl=CaCl2+H2O+CO2↑;复分解反应(合理即可).
点评 本题难度不大,考查学生根据反应原理书写化学方程式、判定反应类型的能力,掌握化学方程式的书写方法(写、配、注、等)、四种基本反应类型的特征即可正确解答本题.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
18.物质的性质决定物质的用途.下列因果关系不成立的是( )
| A. | 因为红磷燃烧能产生白烟,所以可用于制作烟幕弹 | |
| B. | 因为金属钨的熔点高,所以被用来制造灯泡中的灯丝 | |
| C. | 因为氮气化学性质不活泼,所以可用于食品包装袋内防腐 | |
| D. | 因为石墨的导电性,所以可用作高温润滑剂 |
20.下列各项,不会造成水污染的是( )
| A. | 工业“三废”的任意排放 | B. | 生活大量使用含磷洗衣粉 | ||
| C. | 往饮用水加入漂白粉 | D. | 农业上大量施用农药和化肥 |
18.正确运用化学用语是学好化学的基础.请用化学符号完成如表中的空格.
| 2个水分子 | 2个亚铁离子 | 氧化钙中钙元素显+2价 | 铜绿 |
| 2H2O | 2Fe2+ | $\stackrel{+2}{Ca}$O | Cu2(OH)2CO3 |


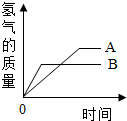 等质量的两种常见金属A和B,分别与足量的稀硫酸反应,生成正二价的金属硫酸盐和氢气.生成氢气的质量与时间关系如图,
等质量的两种常见金属A和B,分别与足量的稀硫酸反应,生成正二价的金属硫酸盐和氢气.生成氢气的质量与时间关系如图,