题目内容
9.下列有关原子的叙述不正确的是( )| A. | 原子是化学变化中不能再分的微粒 | B. | 原子在不断地运动着 | ||
| C. | 原子一定是一种比分子更小的微粒 | D. | 有些原子可以直接构成物质. |
分析 A.根据原子的概念来分析;
B.根据原子的特征来分析;
C.根据原子的体积来分析;
D.根据构成物质的基本粒子来分析.
解答 解:A.原子是化学变化中的最小粒子,故正确;
B.原子在不断地运动,故正确;
C.原子不一定比分子小,故错误;
D.某些物质是由原子直接构成的,如铜是由铜原子构成的,故正确.
故选C.
点评 本题考查了物质构成微粒的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
19.分类是化学研究常用的方法.下列对物质分类正确的是( )
| A. | 氧气(O2)和臭氧(O3)都属于单质 | B. | 氧气(O2)和水(H2O)都属于氧化物 | ||
| C. | 火碱(NaOH)和纯碱(Na2CO3)都属于碱 | D. | 盐酸和氯化氢都是纯净物 |
4.工业铁红的主要成分是Fe2O3,还含有少量的FeO、Fe3O4.现取铁红样品10g与足量的CO反应,测得生成CO2的质量为6.6g,则此铁红中铁元素的质量分数是( )
| A. | 90% | B. | 80% | C. | 76% | D. | 72% |
2.某化学兴趣小组回收利用废旧干电池.
实验1:回收填料中的二氧化锰和氯化铵查阅资料:废旧干电池填料的主要成分为二氧化锰、炭粉、氯化铵和氯化锌等,其中氯化铵、氯化锌可溶于水.兴趣小组的同学们设计回收物质的流程如图1所示.

(1)操作1和操作2的名称都是过滤,该操作中玻璃棒的作用是引流.
(2)灼烧滤渣l的目的是使炭粉和氧气反应转化成二氧化碳,从而和二氧化锰分离
实验2:利用外壳回收物锌制取氢气及相关探究
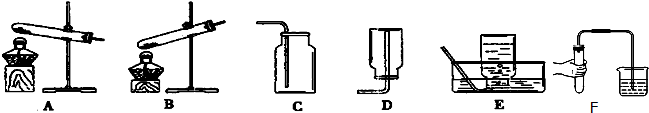
(3)用锌和稀硫酸制取氢气.己知氢气密度比空气小且难溶于水,提供装置如图2.
①应选择:发生装置为B(填编号),排空气法收集装置为D(填编号).
②若用排水法收集并测定气体的体积,气体从装置B导管口b(填“a”或“b”) 进;选用仪器F测量排出水的体积,仪器F名称是量筒.为了保证测定的准确,出水导管应放在仪器F的上端(填“上端”或“底端”).
(4)探究影响锌与稀硫酸反应快慢的因素.反应过程中,用前10min内收集的氢气体积比较反应的快慢.控制其他条件相同,进行下表四组实验,获得数据如表.
①比较实验a和实验b,可以得到的结论是锌越纯,与稀硫酸反应的速率越慢.
②为了研究硫酸浓度对反应快慢的影响,需比较实验a和c(填编号).
③控制其他条件相同,需控制的条件是锌的纯度(列举一种条件即可).
【实验4探究】经处理干净的二氧化锰在氯酸钾分解反应中的催化作用
(1)把干燥纯净的24.5g氯酸钾和5.5g二氧化锰混匀、装入大试管中,加热.
(2)待反应完全后,将试管冷却、称量,得到20.4g残留固体.
(3)再将残留固体经溶解、过滤、洗涤、干燥、称量,得到5.5g黑色固体.
【数据分析】
①该实验说明:二氧化锰在氯酸钾分解反应前后,质量不变.
②完全反应后制得氧气的质量是9.6g.(提示:已知所有化学反应遵循如下规律:参加化学反应的各物质的质量总和等于反应后各生成物的质量总和)
【实验反思】
要证明二氧化锰是氯酸钾分解反应的催化剂,还要做一个对比实验:将等质量的2份氯酸钾粉末,其中一份加入少量的上述实验所得二氧化锰混匀、装入试管,另一份装入另一试管,加热,比较反应速率的大小.
实验1:回收填料中的二氧化锰和氯化铵查阅资料:废旧干电池填料的主要成分为二氧化锰、炭粉、氯化铵和氯化锌等,其中氯化铵、氯化锌可溶于水.兴趣小组的同学们设计回收物质的流程如图1所示.

(1)操作1和操作2的名称都是过滤,该操作中玻璃棒的作用是引流.
(2)灼烧滤渣l的目的是使炭粉和氧气反应转化成二氧化碳,从而和二氧化锰分离
实验2:利用外壳回收物锌制取氢气及相关探究
(3)用锌和稀硫酸制取氢气.己知氢气密度比空气小且难溶于水,提供装置如图2.
①应选择:发生装置为B(填编号),排空气法收集装置为D(填编号).
②若用排水法收集并测定气体的体积,气体从装置B导管口b(填“a”或“b”) 进;选用仪器F测量排出水的体积,仪器F名称是量筒.为了保证测定的准确,出水导管应放在仪器F的上端(填“上端”或“底端”).
(4)探究影响锌与稀硫酸反应快慢的因素.反应过程中,用前10min内收集的氢气体积比较反应的快慢.控制其他条件相同,进行下表四组实验,获得数据如表.
| 验实号编 | 试 剂 | 前 10min 内产生的氢气体积(mL) | |
| 不同纯度的锌 | 不同体积和浓度的稀硫酸 | ||
| a | 纯锌 | 30mL 30% | 564.3 |
| b | 含杂质的锌 | 30mL 30% | 634.7 |
| c | 纯锌 | 30mL 20% | 449.3 |
| d | 纯锌 | 40mL 30% | 602.8 |
②为了研究硫酸浓度对反应快慢的影响,需比较实验a和c(填编号).
③控制其他条件相同,需控制的条件是锌的纯度(列举一种条件即可).
【实验4探究】经处理干净的二氧化锰在氯酸钾分解反应中的催化作用
(1)把干燥纯净的24.5g氯酸钾和5.5g二氧化锰混匀、装入大试管中,加热.
(2)待反应完全后,将试管冷却、称量,得到20.4g残留固体.
(3)再将残留固体经溶解、过滤、洗涤、干燥、称量,得到5.5g黑色固体.
【数据分析】
①该实验说明:二氧化锰在氯酸钾分解反应前后,质量不变.
②完全反应后制得氧气的质量是9.6g.(提示:已知所有化学反应遵循如下规律:参加化学反应的各物质的质量总和等于反应后各生成物的质量总和)
【实验反思】
要证明二氧化锰是氯酸钾分解反应的催化剂,还要做一个对比实验:将等质量的2份氯酸钾粉末,其中一份加入少量的上述实验所得二氧化锰混匀、装入试管,另一份装入另一试管,加热,比较反应速率的大小.
9.推理是一种重要的学习方法,下列推理正确的是( )
| A. | 化学变化都遵循质量守恒定律,所以质量不发生改变的变化就是化学变化 | |
| B. | 化合物是由不同种元素组成的纯净物,所以由不同种元素组成的纯净物一定是化合物 | |
| C. | 置换反应中一定有元素化合价的改变,所以有元素化合价变化的反应一定是置换反应 | |
| D. | 分子、原子都是不带电的微粒,但不带电的微粒不一定都是分子、原子 |
6.小明参观某养鱼池时,好奇的发现农民向养鱼池中撒一种叫做过氧化钙的淡黄色固体,用来增加鱼池中的含氧量.小明刚学完氧气的实验室制法,于是他想可否用?
【提出问题】过氧化钙可否用于制取氧气?
【查阅资料】部分内容如下:过氧化钙(CaO2)室温下稳定,在300℃时分解生成氧气,可做增氧剂、杀菌剂等.
【猜想与论证】
(1)小明依据过氧化钙在300℃时分解生成氧气,提出猜想Ⅰ.
猜想Ⅰ:加热过氧化钙可制取氧气.
实验结论:加热过氧化钙可制取氧气.
(2)小明联想到农民用过氧化钙增加鱼池中的含氧量,提出猜想Ⅱ.猜想Ⅱ:过氧化钙与水反应可制取氧气.
实验结论:不能用过氧化钙与水反应制取氧气.
分析与反思:①虽然没有快速收集到大量氧气,但由此实验现象,小明认为农民用过氧化钙做增氧剂的主要原因是过氧化钙在水中持续、缓慢放出氧气,所以可以作为增氧剂.
②小明希望对些实验进行改进,使该反应加快,你能帮他提出建议吗?你的合理建议:加入催化剂
或加热.以上建议是否可行,还需进一步通过实验验证.
【提出问题】过氧化钙可否用于制取氧气?
【查阅资料】部分内容如下:过氧化钙(CaO2)室温下稳定,在300℃时分解生成氧气,可做增氧剂、杀菌剂等.
【猜想与论证】
(1)小明依据过氧化钙在300℃时分解生成氧气,提出猜想Ⅰ.
猜想Ⅰ:加热过氧化钙可制取氧气.
| 实验装置 | 实验主要过程 |
 | ①检验装置气密性.操作如下:想将导管伸入液面下,用手紧握试管,观察到导管口有气泡冒出,松开后,有液体进入导管. ②加入过氧化钙,加热,导管口有大量气泡冒出. ③收集一瓶气体. ④停止加热.熄灭酒精灯前,应先将导气管从移出水面. |
(2)小明联想到农民用过氧化钙增加鱼池中的含氧量,提出猜想Ⅱ.猜想Ⅱ:过氧化钙与水反应可制取氧气.
| 实验装置 | 实验主要过程 |
 | ①检验装置气密性. ②加入过氧化钙和水后,有少量细小气泡缓慢放出,在导管口几乎看不到气体.该装置放置到第二天,集气瓶中只收集到极少量气体,震荡试管后仍有少量细小气泡缓慢放出. |
分析与反思:①虽然没有快速收集到大量氧气,但由此实验现象,小明认为农民用过氧化钙做增氧剂的主要原因是过氧化钙在水中持续、缓慢放出氧气,所以可以作为增氧剂.
②小明希望对些实验进行改进,使该反应加快,你能帮他提出建议吗?你的合理建议:加入催化剂
或加热.以上建议是否可行,还需进一步通过实验验证.
7.下列关于分子和原子的描述正确的是( )
| A. | 分子可以再分,原子不可再分 | |
| B. | 物质的热胀冷缩是因为分子大小发生改变 | |
| C. | 酒精挥发,分子间间隔会变小 | |
| D. | 原子核不一定都是质子和中子构成的 |
 人们常用肥皂水检验地下水是硬水还是软水;生活中可用煮沸的方法降低水的硬度;如图所示是某同学自制简易净水器,图中活性炭的主要作用是吸附;小卵石、石英砂、蓬松棉的作用是过滤.
人们常用肥皂水检验地下水是硬水还是软水;生活中可用煮沸的方法降低水的硬度;如图所示是某同学自制简易净水器,图中活性炭的主要作用是吸附;小卵石、石英砂、蓬松棉的作用是过滤.