题目内容
17.如图是实验室的部分实验装置,回答有关问题.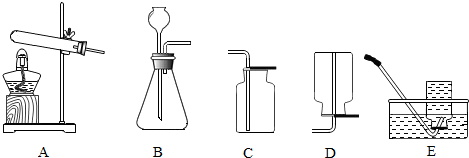
(1)实验室用稀盐酸与石灰石反应制取二氧化碳应选用的装置是(填编号)BC;其中,发生装置中产生CO2的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)检验二氧化碳是否集满的方法是用燃着的木条靠近集气瓶口,观察木条是否熄灭;将适量的澄清的石灰水倒入集气瓶中震荡,观察到试剂变浑浊,说明该气体确实是二氧化碳.
分析 (1)根据石灰石与盐酸反应原理书写方程式,据反应物状态和反应条件选择发生装置;根据气体性质选择收集方法;
(2)根据二氧化碳的性质来分析.
解答 解:(1)用石灰石与稀盐酸反应制取二氧化碳,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;该反应不需加热,属于固液常温型,故选发生装置B;二氧化碳能溶于水,密度比空气大,所以用向上排空气法来收集;故填:BC;CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)利用二氧化碳不燃烧、不支持燃烧的性质来检验二氧化碳是否收集满,可将一根燃着的木条放在集气瓶口,若木条熄灭证明二氧化碳已满;检验二氧化碳气体通常用澄清的石灰水,二氧化碳能使澄清的石灰水变浑浊.故填:用燃着的木条靠近集气瓶口,观察木条是否熄灭;澄清的石灰水.
点评 本题难度不是很大,是中考的重要考点之一,熟练掌握实验室中制取气体的反应原理、发生装置和收集装置的选择依据,检验和验满二氧化碳的方法是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.现有32g某可燃物在密闭容器中完全燃烧后,测得生成88g二氧化碳和72g水,关于该可燃物的说法正确的是( )
| A. | 一定是氧化物 | |
| B. | 只含有碳、氢两种元素 | |
| C. | 一定含有碳、氢、氧三种元素 | |
| D. | 一定含有碳、氢元素,可能含有氧元素 |
8.下列化学方程式书写正确的是( )
| A. | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO | B. | NaOH+H2SO4═Na2SO4+H2O | ||
| C. | CaCO3+2HCL═CaCL2+CO2 | D. | C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ |
5. 硒是人体必需的微量元素.在元素周期表中硒元素的某些信息如图所示,下列有关硒的说法正确的是( )
硒是人体必需的微量元素.在元素周期表中硒元素的某些信息如图所示,下列有关硒的说法正确的是( )
 硒是人体必需的微量元素.在元素周期表中硒元素的某些信息如图所示,下列有关硒的说法正确的是( )
硒是人体必需的微量元素.在元素周期表中硒元素的某些信息如图所示,下列有关硒的说法正确的是( )| A. | 属于金属元素 | B. | 原子序数为34 | ||
| C. | 原子核内中子数为34 | D. | 相对原子质量是78.96g |
12.下列各组物质的溶液,不用其它试剂,仅通过观察和用组内溶液相互混合的方法,不能将它们一一鉴别出来的是( )
| A. | NaOH、Ca(OH)2、HCl、K2CO3 | B. | NaCl、BaCl2、CuSO4、NaOH | ||
| C. | Ba(OH)2、NaCl、Na2SO4、Na2CO3 | D. | AgNO3、HCl、Na2CO3、CaCl2 |
4.维C泡腾片(保健药品)的主要成分有维生素C(C6H9O6)、碳酸氢钠(NaHCO3)和柠檬酸(C6H8O7),它溶于水时,会产生许多气泡
【提出问题】该气体的成分是什么?
【提出猜想】小科认为该气体可能是CO2、O2、CO、H2中的一种或几种,他判断的依据是质量守恒.而小芳认为该气体可能是CO2、O2中的一种或两种,因为从药品安全角度考虑,CO2、H2易燃易爆,且CO有毒,所以不可能含有CO和H2.
【进行实验】
【得出结论】(1)由实验①可知,该气体中肯定含有CO2.
(2)由实验②不能确定该气体中不含氧气,理由是如果氧气的浓度较小时不能使带火星的木条复燃,同时二氧化碳不支持燃烧.
【提出问题】该气体的成分是什么?
【提出猜想】小科认为该气体可能是CO2、O2、CO、H2中的一种或几种,他判断的依据是质量守恒.而小芳认为该气体可能是CO2、O2中的一种或两种,因为从药品安全角度考虑,CO2、H2易燃易爆,且CO有毒,所以不可能含有CO和H2.
【进行实验】
| 试验编号 | 实验操作 | 实验现象 |
| ① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
| ② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
(2)由实验②不能确定该气体中不含氧气,理由是如果氧气的浓度较小时不能使带火星的木条复燃,同时二氧化碳不支持燃烧.
11.学生在做“酸、碱、盐之间能否反应”的探究实验时,用到了H2SO4、Ba(NO3)2、KOH 和 K2CO3 四种溶液.实验结束后,所有的废液集中在一个大烧杯中,观察到废液呈白色浑浊.为了防止污染环境,化学实验小组将废液进行过滤.
【对滤渣的猜想】
小东认为:滤渣中只有 BaSO4.
小西认为:滤渣中只有 BaCO3.
你认为:滤渣中含有BaSO4 和BaCO3 .
【实验探究一】证明你自己的猜想成立的操作方法和现象是:
【对滤液的猜想】小青认为:滤液中含有KNO3、K2CO3、KOH.
小黄认为:滤液中含有KNO3、K2SO4、H2SO4.
小兰认为:滤液中含有KNO3、Ba(NO3)2、KOH.
小红认为:滤液中含有KNO3、K2SO4、Ba(NO3)2、KOH.
大家讨论后一致认为小红的猜想一定不成立,理由是:Ba(NO3)2+Na2SO4═BaSO4↓+2NaNO3(用化学方程式表示).
【资料提供】K2CO3溶液显碱性.
【实验探究二】

【实验现象及结论】
(1)根据实验①,小黄的猜想不成立.
(2)根据实验②,若小兰的猜想不成立,现象a为没有白色沉淀.
(3)根据实验③,若小青的猜想成立,X溶液可能是CaCl2溶液,现象b为溶液变红色.
【对滤渣的猜想】
小东认为:滤渣中只有 BaSO4.
小西认为:滤渣中只有 BaCO3.
你认为:滤渣中含有BaSO4 和BaCO3 .
【实验探究一】证明你自己的猜想成立的操作方法和现象是:
| 实验操作 | 实验现象 |
| 取少量滤渣于试管中,加入足量 稀盐酸 | 固体部分溶解,有气泡冒出 |
小黄认为:滤液中含有KNO3、K2SO4、H2SO4.
小兰认为:滤液中含有KNO3、Ba(NO3)2、KOH.
小红认为:滤液中含有KNO3、K2SO4、Ba(NO3)2、KOH.
大家讨论后一致认为小红的猜想一定不成立,理由是:Ba(NO3)2+Na2SO4═BaSO4↓+2NaNO3(用化学方程式表示).
【资料提供】K2CO3溶液显碱性.
【实验探究二】

【实验现象及结论】
(1)根据实验①,小黄的猜想不成立.
(2)根据实验②,若小兰的猜想不成立,现象a为没有白色沉淀.
(3)根据实验③,若小青的猜想成立,X溶液可能是CaCl2溶液,现象b为溶液变红色.