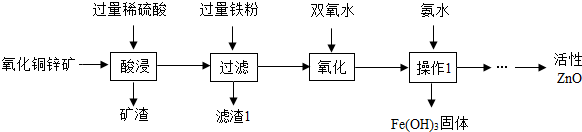
题目内容
8.化学兴趣小组的同学将足量的锌粒加入到浓硫酸中,发现有大量的气泡放出,他们对气体的成分进行了探究.【提出问题】锌粒加入浓硫酸后生成的气体是什么?
【查阅资料】
①浓硫酸能与锌反应,但不产生氢气,也不会产生氧气;
②SO2有刺激性气味,易溶于水,能使品红(一种红色色素)溶液褪色.
【提出猜想】
甲:气体是H2;
乙:气体是SO2;
丙:气体是SO2和H2;
【实验探究】
为了验证上述猜想.同学们在老师的指导下设计了如下图的装置(部分夹持器材略去,假设每个能发生的反应都完全进行)进行探究:
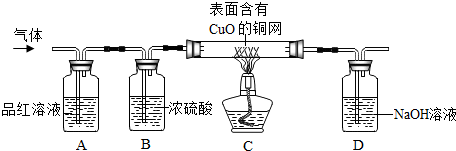
(1)实验开始后,观察到A中品红溶液褪色,证明气体中含有SO2.
(2)B装置的作用是除去混合气体中的水蒸气.
(3)C装置在点燃酒精灯加热之前应先通一段时间的气体,目的是排出玻璃管中的空气;加热一段时间后,观察到黑色物质变成红色,证明气体中含有H2.
(4)写出D瓶中发生的反应的化学方程式SO2+2NaOH═Na2SO3+H2O.
【讨论】
(1)锌和浓硫酸反应生成硫酸锌、水和二氧化硫,为什么在反应过程中又产生了氢气呢?用文字简述原因:随着反应的进行,浓硫酸逐渐变为稀硫酸.
(2)锌与浓硫酸和稀硫酸反应都可以产生硫酸锌,如果需要制取硫酸锌,用锌与稀硫酸反应的优点是不生成污染环境的SO2(任填一种合理的答案).
分析 (1)根据题干资料分析;
(2)根据浓硫酸具有吸水性分析;
(3)由于氢气与空气混合在加热时可能出现爆炸,氢气能与氧化铜反应生成铜和水;
(4)二氧化硫与氢氧化钠反应生成亚硫酸钠和水;
【讨论】
(1)根据锌与稀硫酸反应生成氢气分析;
(2)根据二氧化硫会造成空气的污染分析.
解答 解:(1)由资料“SO2有刺激性气味,易溶于水,能使品红(一种红色色素)溶液褪色”可知,观察到A中品红溶液褪色,证明气体中含有SO2;
(2)由于浓硫酸具有吸水性,所以B装置中的浓硫酸可以除去混合气体中的水蒸气;
(3)由于氢气与空气混合在加热时可能出现爆炸,因此,在进行加热前要把玻璃管中空气全部排出,所以进行操作时应先通入氢气排出管内空气然后再进行加热;氢气能与氧化铜反应生成铜和水,会观察到会黑色粉末变红;
(4)反应中生成的二氧化硫会造成空气的污染,所以用氢氧化钠溶液吸收,二氧化硫与氢氧化钠反应生成亚硫酸钠和水,化学方程式为:SO2+2NaOH═Na2SO3+H2O;
【讨论】
(1)随着反应的进行,浓硫酸逐渐变为稀硫酸,锌与稀硫酸反应生成氢气;
(2)锌和浓硫酸反应生成硫酸锌、水和二氧化硫,锌和稀硫酸反应生成硫酸锌、水,不生成污染环境的SO2等.
故答案为:(1)SO2
(2)除去混合气体中的水蒸气;
(3)排出玻璃管中的空气;黑色物质变成红色;
(4)SO2+2NaOH═Na2SO3+H2O
【讨论】
(1)随着反应的进行,浓硫酸逐渐变为稀硫酸
(2)不生成污染环境的SO2(或“可以节约药品”)(其它合理答案均可)
点评 解答本题的关键是要充分理解实验装置的特点和各种物质的性质,只有这样才能对问题做出正确的判断.

练习册系列答案
相关题目
16.下列化学用语与含义相符的是( )
| A. | 3H-3个氢元素 | B. | O-1个氧分子 | C. | Na-1个钠原子 | D. | Mg+2-1个镁离子 |
13.某纯净物X在空气中完全燃烧,反应的化学方程式为:X+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O,下列关于X的说法正确的是( )
| A. | X由碳、氢、氧三种元素组成 | B. | X的相对分子质量为10 | ||
| C. | X中碳、氢元素的质量比为1:4 | D. | X属于有机化合物 |
20.南昌汉代海昏侯墓出土的文物中,保存完好的玉器非常罕见.对玉石主要成分(化学式为NaAlSi2O6)的描述正确的是( )
| A. | 含有3个氧分子 | B. | 相对分子质量为94 | ||
| C. | 钠元素的质量分数为13.4% | D. | 钠元素与铝元素的质量比为23:27 |
17.下列化学的方程式符合题意且书写正确的是( )
| A. | 工业上用高温煅烧石灰石的方法制生石灰:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+H2O | |
| B. | 医疗上用氢氧化镁中和过多胃酸:Mg(OH)2+HCl═MgCl2+H2O | |
| C. | 除去铜中少量铁粉的方法之一:2Fe+6HCl═2FeCl3+3H2↑ | |
| D. | 正常雨水的pH约为5.6的原因:CO2+H2O═H2CO3 |
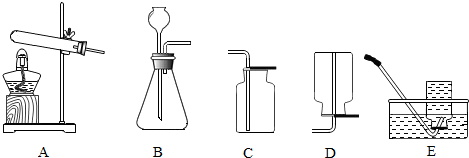
 人类的日常生活和工农业生产都离不开水,请回答:
人类的日常生活和工农业生产都离不开水,请回答: