题目内容
6.研究性学习小组研究从空气中制取氮气,以下是他们设计的实验方案:
(1)空气通过图1装置可除去二氧化碳和水蒸气,空气应该从B端通入(填“A”或“B”).

(2)除去氧气:他们分别收集一瓶气体用图2装置进行除去氧气的燃烧实验,其中甲同学选用红磷,乙同学选用硫粉.你认为:不能选用硫粉 (填“红磷”或“硫粉”),原因是硫燃烧生成二氧化硫气体,会使制得的氮气不纯净.不能选用的反应的符号表达式为S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.
(3)分析误差:此法得到的氮气密度(标准状况下)与氮气的实际密度有误差.出现误差的可能原因(写两种,不考虑计算错误):①二氧化碳(或水蒸汽、氧气)没有除尽;②稀有气体没有除去.
分析 (1)利用氢氧化钠可与二氧化碳反应、浓硫酸可吸收水的性质,达到除去二氧化碳和水蒸气实验目的;
(2)根据除去杂质的基本原则:不引入新的杂质,分析两种除去氧气方案的可行性,说明不可行方案不可行的理由;
(3)与氮气实际密度有误差,说明所得氮气不纯,试分析造成氮气不纯的原因.
解答 解:(1)利用氢氧化钠溶液与二氧化碳反应生成碳酸钠和水而除去二氧化碳,所以应该从长导气管进,从短导气管出;
(2)由于硫和氧气反应会生成气体二氧化硫,因此在除去氧气的同时又引入了新的气体杂质二氧化碳,所以乙同学方案不科学;
(3)分析以上操作,会发现空气中的氧气、二氧化碳、水蒸气被除去,但空气中含量很少的稀有气体并没有除去,因此由于氮气中混有稀有气体而使氮气不纯,密度与实际密度有误差;另外,在使用红磷除去氧气时,可能由于某种原因而没有把氧气完全除去而使所得氮气不纯,密度与实际密度有误差.
故答案为:(1)B;
(2)硫粉;硫燃烧生成二氧化硫气体,会使制得的氮气不纯净;S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2;
(3)①二氧化碳(或水蒸汽、氧气)没有除尽;②稀有气体没有除去.
点评 本题主要考查实验方案的设计与评价,物质的除杂和分离混合物的方法,重点联系空气中氧气含量测定实验进行分析.

练习册系列答案
相关题目
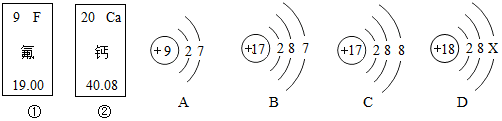
17.空气中含量较高且性质活泼的气体是( )
| A. | 氮气 | B. | 水蒸气 | C. | 二氧化碳 | D. | 氧气 |
14.硼氢化钠(NaBH4,其中氢元素的化合价为-1),是一种安全车载氢源.有关硼氢化钠的说法正确的是( )
| A. | 含2个氢分子 | B. | 只含一种非金属元素 | ||
| C. | 硼元素的化合价为+3 | D. | Na、B、H的质量比为1:1:4 |
1.下列关于水(H2O)和双氧水(H2O2)的说法正确的是( )
| A. | 都含有两个氢原子 | B. | 都含有氢气 | ||
| C. | 都含有氢分子 | D. | 都含有氢元素 |
11.下列物质的鉴别方法不正确的是( )
| A. | 空气与氧气--带火星的木条 | B. | 硬水与软水--观察颜色 | ||
| C. | 二氧化碳和氮气--澄清石灰水 | D. | 铜丝与铁丝--用磁铁吸引 |
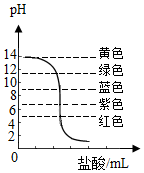 化学兴趣小组在马老师的指导下,借助紫甘蓝汁液进行中和反应实验.
化学兴趣小组在马老师的指导下,借助紫甘蓝汁液进行中和反应实验.
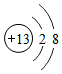 它属于金属元素(填“金属元素”或“非金属元素”或“稀有气体元素”),该微粒的符号为Al;该结构是(填是或不是)稳定结构.
它属于金属元素(填“金属元素”或“非金属元素”或“稀有气体元素”),该微粒的符号为Al;该结构是(填是或不是)稳定结构.