题目内容
(2011?攀枝花)氯化钠是一种重要的化工原料.电解氯化钠溶液可制得氯气、氢氧化钠等物质,反应的化学方程式为2NaCl+2H2O Cl2↑+H2↑+2NaOH.现取一定质量的氯化钠溶液进行电解,当氯化钠恰好完全反应时,得到51.2g溶液,生成氯气的质量与时间的关系如右图所示.请计算:
Cl2↑+H2↑+2NaOH.现取一定质量的氯化钠溶液进行电解,当氯化钠恰好完全反应时,得到51.2g溶液,生成氯气的质量与时间的关系如右图所示.请计算:(1)氯化钠完全反应时,溶液中剩余水的质量.
(2)原氯化钠溶液中溶质的质量分数.
(3)若把这些氯化钠溶液稀释成溶质的质量分数为0.9%的生理盐水,需要加水的质量.

【答案】分析:据图可看出,氯化钠完全反应时可得到氯气7.1g.
(1)反应结束后所得溶液内包含氢氧化钠和水,根据氯气的质量可求出氢氧化钠的质量,再用反应结束后所得溶液的质量-氢氧化钠的质量即为溶液中剩余水的质量.
(2)原氯化钠溶液中溶质的质量分数= %,氯化钠的质量可根据氯气的质量算出,根据质量守恒定律,氯化钠溶液的质量=氯气的质量+氢气的质量(可根据氯气的质量算出)+反应结束后所得溶液的质量.
%,氯化钠的质量可根据氯气的质量算出,根据质量守恒定律,氯化钠溶液的质量=氯气的质量+氢气的质量(可根据氯气的质量算出)+反应结束后所得溶液的质量.
(3)根据稀释前后溶液中溶质的质量不变列出等式.
解答:解:(1)设消耗氯化钠的质量为x,生成氢氧化钠的质量为y,生成氢气的质量为z
2NaCl+2H2O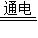 Cl2↑+H2↑+2NaOH
Cl2↑+H2↑+2NaOH
117 71 2 80
x 7.1g z y
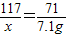
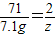
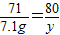
x=11.7g z=0.2g y=8g
剩余水的质量:51.2g-8g=43.2g
答:溶液中剩余水的质量为43.2g
(2)氯化钠溶液质量为:51.2g+7.1g+0.2g=58.5g
氯化钠溶液中溶质的质量分数为: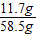 ×100%=20%
×100%=20%
答:原氯化钠溶液中溶质的质量分数为20%.
(3)设稀释后生理盐水的质量为a
58.5 g×20%=a×0.9%
a=1300 g
需要加水的质量为:1300 g-58.5 g=1241.5 g
答若把这些氯化钠溶液稀释成0.9%的生理盐水,需要加水的质量为1241.5 g.
点评:稀释溶液的过程只是加水的过程,稀释前后溶液中溶质的质量不变,因此在做有关稀释溶液的计算题时可根据稀释前后溶液中溶质的质量不变列出等式.
(1)反应结束后所得溶液内包含氢氧化钠和水,根据氯气的质量可求出氢氧化钠的质量,再用反应结束后所得溶液的质量-氢氧化钠的质量即为溶液中剩余水的质量.
(2)原氯化钠溶液中溶质的质量分数=
 %,氯化钠的质量可根据氯气的质量算出,根据质量守恒定律,氯化钠溶液的质量=氯气的质量+氢气的质量(可根据氯气的质量算出)+反应结束后所得溶液的质量.
%,氯化钠的质量可根据氯气的质量算出,根据质量守恒定律,氯化钠溶液的质量=氯气的质量+氢气的质量(可根据氯气的质量算出)+反应结束后所得溶液的质量.(3)根据稀释前后溶液中溶质的质量不变列出等式.
解答:解:(1)设消耗氯化钠的质量为x,生成氢氧化钠的质量为y,生成氢气的质量为z
2NaCl+2H2O
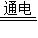 Cl2↑+H2↑+2NaOH
Cl2↑+H2↑+2NaOH117 71 2 80
x 7.1g z y
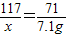
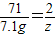
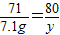
x=11.7g z=0.2g y=8g
剩余水的质量:51.2g-8g=43.2g
答:溶液中剩余水的质量为43.2g
(2)氯化钠溶液质量为:51.2g+7.1g+0.2g=58.5g
氯化钠溶液中溶质的质量分数为:
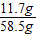 ×100%=20%
×100%=20%答:原氯化钠溶液中溶质的质量分数为20%.
(3)设稀释后生理盐水的质量为a
58.5 g×20%=a×0.9%
a=1300 g
需要加水的质量为:1300 g-58.5 g=1241.5 g
答若把这些氯化钠溶液稀释成0.9%的生理盐水,需要加水的质量为1241.5 g.
点评:稀释溶液的过程只是加水的过程,稀释前后溶液中溶质的质量不变,因此在做有关稀释溶液的计算题时可根据稀释前后溶液中溶质的质量不变列出等式.

练习册系列答案
相关题目
(2011?攀枝花)碳酸氢钠常用于食品和医药工业.某化学兴趣小组的同学对碳酸氢钠的热稳定性进行探究.
【查阅资料】
1.碳酸氢钠受热容易分解,生成水、二氧化碳气体和一种______常见的固体物质.
2.碳酸钠溶液呈碱性.
【进行实验】
为了验证碳酸氢钠受热时会分解,兴趣小组的同学取一定质量的碳酸氢钠到铜片上加热,如右上图所示.
(1)加热一段时间后,观察到烧杯内壁有______.
(2)充分加热后,将烧杯迅速倒转过来,倒入适量的澄清石灰水,振荡,观察到石灰水变浑浊.写出该反应的化学方程式:______.
(3)兴趣小组的同学认为:充分加热后的固体产物可能是NaOH或Na2CO3.
①他们的依据是______.
②兴趣小组为了确定反应后的固体产物成分进行以下实验,请填写下表:
【讨论与评价】实验一的结论与实验二、实验三的结论相反,在讨论时,兴趣小组的同学认为方案一的结论不正确,他们的理由是______.
【总结】请写出碳酸氢钠受热分解的化学方程式______ Na2CO3+CO2↑+H2O

【查阅资料】
1.碳酸氢钠受热容易分解,生成水、二氧化碳气体和一种______常见的固体物质.
2.碳酸钠溶液呈碱性.
【进行实验】
为了验证碳酸氢钠受热时会分解,兴趣小组的同学取一定质量的碳酸氢钠到铜片上加热,如右上图所示.
(1)加热一段时间后,观察到烧杯内壁有______.
(2)充分加热后,将烧杯迅速倒转过来,倒入适量的澄清石灰水,振荡,观察到石灰水变浑浊.写出该反应的化学方程式:______.
(3)兴趣小组的同学认为:充分加热后的固体产物可能是NaOH或Na2CO3.
①他们的依据是______.
②兴趣小组为了确定反应后的固体产物成分进行以下实验,请填写下表:
| 实验 | 实验现象 | 结论 |
| 实验一:取少量反应后的固体产物溶于水,滴入几滴酚酞试液 | 溶液变成红色 | 固体产物是NaOH,而不是Na2CO3 |
| 实验二:取少量反应后的固体产物溶于水,加入过量氯化钙溶液 | ______ | 固体产物是Na2CO3,而不是NaOH |
| 实验三:______ | 产生大量气泡 | 固体产物是Na2CO3,而不是NaOH |
【总结】请写出碳酸氢钠受热分解的化学方程式______ Na2CO3+CO2↑+H2O

 ,氯原子的最外层电子数为.下列图中微粒共表示种元素,其中与氯原子具有相似化学性质的是(填序号).
,氯原子的最外层电子数为.下列图中微粒共表示种元素,其中与氯原子具有相似化学性质的是(填序号).
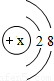 ,则x的数值可能是下列中的.
,则x的数值可能是下列中的.