题目内容
10.水在生活、生产和化学实验中起着十分重要的作用
(1)自来水厂净化水的过程为:取水→过滤→吸附→消毒,高铁酸钾(K2FeO4)能用作絮凝剂,制备K2FeO4的化学方程式为:2Fe(OH)3+3Cl2+10KOH═2K2FeO4+6X+8H2O,则X的化学式为KCl,K2FeO4中铁元素的化合价为+6.
(2)水通入直流电后可分解,以下图片是水分解过程中微粒变化的部分示意图,A、B、C三张图片中,C是反应物,A图片说明在化学反应中分子可以再分,写出反应的化学方程式2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
分析 (1)根据质量守恒定律解答;根据在化合物中正负化合价代数和为零,结合高铁酸钾的化学式进行解答本题.
(2)根据化学反应的实质进行分析,根据水通电分解生成氢气和氧气书写方程式.
解答 解:(1)根据反应的化学方程式:2Fe(OH)3+3Cl2+10KOH═2K2FeO4+6X+8H2O,反应物中铁、氧、钾、氢、氯原子个数分别为2、16、10、16、6,反应后的生成物中铁、氧、钾、氢、氯原子个数分别为2、16、4、16、0,根据反应前后原子种类、数目不变,则6X中含有6个钾原子和6个氯原子,则每个X分子由1个钾原子和1个氯原子构成,则物质X的化学式为KCl.
在K2FeO4中,钾元素显+1价,氧元素显-2价,设铁元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+(-2)×4=0,则x=+6价.
(2)根据图示可知,C是水,是反应物;由化学反应的实质可知:化学反应的过程就是参加反应的各物质的原子,重新组合生成其他物质的过程,所以,水分解生成氢气和氧气的过程就是水分子分解为氢原子和氧原子,每两个氢原子构成以一个氢分子,每两个氧原子构成一个氧分子;电解水生成氢气和氧气,反应的化学方程式为:2H2O $\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
故答案为:
(1)KCl;+6;
(2)C;分子;2H2O $\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
点评 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
20.某兴趣小组的同学为了探究化学反应前后反应物与生成物之间的质量关系设计了如下三个实验:
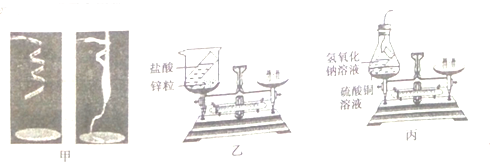
实验甲:称量镁条,在空气中点燃,待反应结束后,将生成物全部收回再称量.
实验乙:将装有稀盐酸的小试管放入装有锌粒的烧杯中,称量,然后将盐酸与锌粒接触,过一会再称量.(化学方程式是:Zn+2HCl=ZnCl2+H2↑)
实验丙:将装有氢氧化钠溶液的试管放入盛有硫酸铜的锥形瓶中,并在锥形瓶口塞上橡皮塞,称量,然后设法将两种溶液接触,过一会再称量.(化学方程式是:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4)
他们得到三次实验的数据如表:
(1)在实验甲中反应后的质量比反应前明显增加了,请解释原因:镁燃烧时,和空气中的氧气反应生成了氧化镁,因此氧化镁的质量大于反应的镁的质量.
(2)由上表中数据分析可知实验甲中参加反应的氧气质量为3.2g,实验乙中生成氢气的质量为0.2g.
(3)在上述三个实验中都遵循(填“遵循”或者“不遵循”)质量守恒定律,但只有实验丙正确反映了反应物与生成物之间的总质量关系,因此,用实验来探究化学反应前后反应物与生成物之间的总质量关系时,当有气体参加或生成时,必须在密闭容器中进行.
(4)请从分子、原子的角度解释反应前后质量相等的原因:反应前后原子的种类、总个数、质量都不变.
(5)在化学反应前后,肯定不会变化的是①③④.
①原子的数目 ②分子的数目 ③元素的种类 ④物质的质量总和 ⑤物质的种类 ⑥物质的体积 ⑦物质的状态
(6)质量守恒定律这条结论的获得对化学研究的重大意义在于可以定量进行化学反应.

实验甲:称量镁条,在空气中点燃,待反应结束后,将生成物全部收回再称量.
实验乙:将装有稀盐酸的小试管放入装有锌粒的烧杯中,称量,然后将盐酸与锌粒接触,过一会再称量.(化学方程式是:Zn+2HCl=ZnCl2+H2↑)
实验丙:将装有氢氧化钠溶液的试管放入盛有硫酸铜的锥形瓶中,并在锥形瓶口塞上橡皮塞,称量,然后设法将两种溶液接触,过一会再称量.(化学方程式是:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4)
他们得到三次实验的数据如表:
| 编号 | 实验甲 | 实验乙 | 实验丙 |
| 反应前/g | 4.8 | 112.6 | 118.4 |
| 反应后/g | 8.0 | 112.4 | 118.4 |
(2)由上表中数据分析可知实验甲中参加反应的氧气质量为3.2g,实验乙中生成氢气的质量为0.2g.
(3)在上述三个实验中都遵循(填“遵循”或者“不遵循”)质量守恒定律,但只有实验丙正确反映了反应物与生成物之间的总质量关系,因此,用实验来探究化学反应前后反应物与生成物之间的总质量关系时,当有气体参加或生成时,必须在密闭容器中进行.
(4)请从分子、原子的角度解释反应前后质量相等的原因:反应前后原子的种类、总个数、质量都不变.
(5)在化学反应前后,肯定不会变化的是①③④.
①原子的数目 ②分子的数目 ③元素的种类 ④物质的质量总和 ⑤物质的种类 ⑥物质的体积 ⑦物质的状态
(6)质量守恒定律这条结论的获得对化学研究的重大意义在于可以定量进行化学反应.
5.同学们分别取6g固体和20mL水,研究物质溶解前后温度的变化.
(1)由于NaOH有腐蚀性,称量时应将NaOH固体放在烧杯中.
(2)实验③中可观察到的温度变化是温度降低.
(3)三个实验中,固体和水的用量相同,这样做的目的是控制变量,对比三种物质溶解前后的温度变化.
| 实验序号 | ① | ② | ③ |
| 实验内容 |  |  |  |
| 温度变化 | 温度升高 | 基本不变 | 温度降低 |
(2)实验③中可观察到的温度变化是温度降低.
(3)三个实验中,固体和水的用量相同,这样做的目的是控制变量,对比三种物质溶解前后的温度变化.
15.下列实验操作正确的是( )
| A. |  倾倒液体 | B. |  加热液体 | C. |  量取液体 | D. |  滴加液体 |
20.物质的性质决定用途.下列用途主要是利用其化学性质的是( )
| A. |  活性炭净水 | B. |  金刚石作装饰品 | C. |  铜丝作导线 | D. |  氢气作高能燃料 |

 在现代农业园,同学们学习到以下知识:
在现代农业园,同学们学习到以下知识: 如图中的物质为初中化学常见物质,他们之间的反应关系如图所示(“→”表示转化关系,“-”表示相互能反应,部分反应物、生成物或反应条件已略去).人的胃液中含有少量的A可帮助消化,A、B发生中和反应,产物之一是厨房内常用的调味品;C常用于改良酸性土壤,D为碳酸盐,且C的溶液与D的溶液反应可得到B;F和G在常温下都为气体.请回答:
如图中的物质为初中化学常见物质,他们之间的反应关系如图所示(“→”表示转化关系,“-”表示相互能反应,部分反应物、生成物或反应条件已略去).人的胃液中含有少量的A可帮助消化,A、B发生中和反应,产物之一是厨房内常用的调味品;C常用于改良酸性土壤,D为碳酸盐,且C的溶液与D的溶液反应可得到B;F和G在常温下都为气体.请回答: