题目内容
13.现有77mL,溶质的质量分数为40%的硫酸溶液和66.67mL,溶质的质量分数为60%的硫酸溶液,将它们两两混合后,所得溶液的溶质质量分数是多少?(已知质量分数为40%的H2SO4的密度为1.30g•cm-3,质量分数为60%的H2SO4的密度为1.50g•cm-3)分析 根据题意,结合溶质质量=溶液质量×溶质的质量分数,溶质的质量分数=$\frac{溶质质量}{溶液质量}$×100%,进行分析解答即可.
解答 解:由于1mL=1cm3
77mL溶质的质量分数为40%的硫酸溶液的质量为77cm3×1.30g•cm-3=100.10g;
66.67mL溶质的质量分数为60%的硫酸溶液的质量为66.67cm3×1.50g•cm-3=100.01g;
77mL溶质的质量分数为40%的硫酸溶液和66.67mL溶质的质量分数为60%的硫酸溶液,将它们两两混合后,所得溶液的溶质质量分数是将20g溶质质量分数为$\frac{100.10g×40%+100.01g×60%}{100.10g+100.01g}$×100%≈50.00%.
答:所得溶液的溶质质量分数是50.00%.
点评 本题难度不大,掌握溶质质量=溶液质量×溶质的质量分数、溶质的质量分数=$\frac{溶质质量}{溶液质量}$×100%并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
3.化学是一门研究物质的科学,我们一般从物质的存在、性质、制备、用途等方面研究一种物质或一类物质.以金属为例,请你参与其中回答相关问题:
(1)认识金属元素存在:自然界中大多数金属都以化合物的形式存在.下列矿石的主要成分属于氧化物的是AD(填字母序号,下同);
A.铝土矿(主要成分A12O3) B.辉铜矿(主要成分Cu2S)
C.菱铁矿(主要成分FeCO3) D.磁铁矿(主要成分Fe3O4)
(2)探究金属物理性质:
如表是A、B、C三种金属的部分物理性质.
①高压输电线不用金属A而选用金属B,主要原因是金属B的密度比A小.
②C的合金通常可以做菜刀、锤子等,其合金的硬度>5(填“>”“<”或“=”).
(3)探究金属化学性质:
材料:我国第四套人民币中的一元硬币是钢芯镀镍(Ni),镍与稀硫酸能发生下列反应:
Ni+H2SO4═NiSO4+H2↑.
写出Ni与CuSO4溶液发生置换反应的方程式Ni+CuSO4═Cu+NiSO4.
(4 )认识金属的制备:工业上常采用还原法、置换法、电解法制备金属.用一氧化碳还原赤铁矿冶铁反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(1)认识金属元素存在:自然界中大多数金属都以化合物的形式存在.下列矿石的主要成分属于氧化物的是AD(填字母序号,下同);
A.铝土矿(主要成分A12O3) B.辉铜矿(主要成分Cu2S)
C.菱铁矿(主要成分FeCO3) D.磁铁矿(主要成分Fe3O4)
(2)探究金属物理性质:
如表是A、B、C三种金属的部分物理性质.
| 性质 金属 | 导电性(100为标准) | 密度(g/cm3) | 熔点(℃) | 硬度(10为标准) |
| A | 99 | 8.92 | 1083 | 3 |
| B | 61 | 2.70 | 660 | 2.9 |
| C | 17 | 7.86 | 1535 | 5 |
②C的合金通常可以做菜刀、锤子等,其合金的硬度>5(填“>”“<”或“=”).
(3)探究金属化学性质:
材料:我国第四套人民币中的一元硬币是钢芯镀镍(Ni),镍与稀硫酸能发生下列反应:
Ni+H2SO4═NiSO4+H2↑.
写出Ni与CuSO4溶液发生置换反应的方程式Ni+CuSO4═Cu+NiSO4.
(4 )认识金属的制备:工业上常采用还原法、置换法、电解法制备金属.用一氧化碳还原赤铁矿冶铁反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
4.当燃着的小木条燃烧端朝上时,木条没烧完就会熄灭,原因是( )
| A. | 缺乏氧气 | |
| B. | 缺乏可燃物 | |
| C. | 小木条的着火点升高了 | |
| D. | 燃烧端下面的小木条温度不宜达到其着火点 |
3.某化学兴趣小组的同学利用过氧化氮分解来探究影响化学反应速率的因素,他们设计如下的实验,并记录了相关数据:
(1)在上述实验中二氧化锰起催化作用.
(2)写出该实验涉及反应的文字表达式:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
(3)通过实验①②对比可知,化学反应速率与过氧化氢浓度有关;从实验②③对比可知,化学反应速率与温度有关.
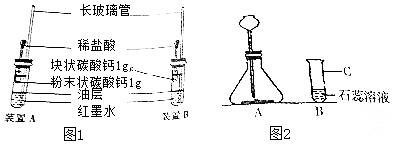
(4)同学们设计了如图1所示的装置进行实验,其中量筒的作用是根据进入量筒中水的体积判断生成的氧气的体积;在第四组实验中,出现了胶塞弹飞和试剂喷出的现象,导致该现象出现的原因可能是过氧化氢浓度越大则反应越剧烈.

(5)实验过程中同学们发现很难控制反应的温度,反应进行一段时间后溶液的温度总是比起始温度高,说明该反应放出热量.
(6)同学们通过记录并分析实验数据发现,过氧化氢分解的速率先增大后减小,如图2所示.请你帮他们解释其原因:反应放热能加快反应,随着反应的进行过氧化氢浓度降低,反应逐渐减慢.过氧化氢分解的快慢还可能受哪些因素影响呢?请你再举出两种因素:催化剂的种类;;催化剂的颗粒大小(催化剂的用量、是否用催化剂等).
| 实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液体积/mL | 二氧化锰的用量/g | 温度/℃ | 收集氧气的体积/mL | 反应所需的时间/s |
| ① | 5 | 2 | 0.1 | 20 | 20 | 48 |
| ② | 10 | 2 | 0.1 | 20 | 20 | 30 |
| ③ | 10 | 2 | 0.1 | 40 | 20 | 18 |
| ④ | 15 | 2 | 0.1 | 60 | 20 | 6 |
(2)写出该实验涉及反应的文字表达式:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
(3)通过实验①②对比可知,化学反应速率与过氧化氢浓度有关;从实验②③对比可知,化学反应速率与温度有关.
(4)同学们设计了如图1所示的装置进行实验,其中量筒的作用是根据进入量筒中水的体积判断生成的氧气的体积;在第四组实验中,出现了胶塞弹飞和试剂喷出的现象,导致该现象出现的原因可能是过氧化氢浓度越大则反应越剧烈.

(5)实验过程中同学们发现很难控制反应的温度,反应进行一段时间后溶液的温度总是比起始温度高,说明该反应放出热量.
(6)同学们通过记录并分析实验数据发现,过氧化氢分解的速率先增大后减小,如图2所示.请你帮他们解释其原因:反应放热能加快反应,随着反应的进行过氧化氢浓度降低,反应逐渐减慢.过氧化氢分解的快慢还可能受哪些因素影响呢?请你再举出两种因素:催化剂的种类;;催化剂的颗粒大小(催化剂的用量、是否用催化剂等).
10.下列叙述、对应的化学方程式、所属基本反应类型都正确的是( )
| A. | 石笋、石柱形成的原因:Ca(HCO3)2=CaCO3↓+CO2↑+H2O分解反应 | |
| B. | 医疗上用小苏打治疗胃酸过多症Na2CO3+2HCl=2NaCl+H2O+CO2↑复分解反应 | |
| C. | 用熟石灰中和硫酸厂废水Ca(OH)2+H2SO4=CaSO4+2H2O中和反应 | |
| D. | 用铁丝测定空气中氧气的含量3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$ Fe3O4 化合反应 |
7.下列叙述正确的是( )
| A. | 水结冰后分子停止运动 | |
| B. | 氯化钠晶体由氯化钠分子构成 | |
| C. | 氢原子和氧原子保持氯化氢的化学性质 | |
| D. | 氧化汞分子在化学变化中能够再分 |