题目内容
15. 为测定某硫酸溶液的溶质质量分数,某同学取10g样品,逐滴加入溶质质量分数为5%的NaOH溶液,边加入边搅拌,溶液pH的变化如图所示,请回答下列问题:
为测定某硫酸溶液的溶质质量分数,某同学取10g样品,逐滴加入溶质质量分数为5%的NaOH溶液,边加入边搅拌,溶液pH的变化如图所示,请回答下列问题:(1)n点所对应的溶液中所含阴离子符号为SO42-;
(2)图中m点所消耗氢氧化钠溶液中溶质的质量为0.8g;
(3)计算该硫酸的溶质质量分数(请写出计算过程).
分析 (1)根据溶液的pH、稀H2SO4与NaOH溶液的反应分析溶液中存在的离子;
(2)根据溶质质量分数的计算公式计算;
(3)根据稀H2SO4与NaOH溶液的反应的方程式,由NaOH的质量求出稀H2SO4的溶质稀H2SO4的溶质质量分数,再求出稀H2SO4的溶质质量分数.
解答 解:(1)由图示可知,在n点时溶液的pH小于7,说明加入的NaOH完全反应,有剩余的硫酸,所以,溶液中含有的阴离子为:SO42-;
(2)由图示可知,在m点时溶液的pH等于7,消耗的NaOH溶液的质量为16g,溶质的质量为:16g×5%=0.8g;
(3)10g稀硫酸样品含有H2SO4的质量为x
2NaOH+H2SO4═Na2SO4+2H2O
80 98
0.8g x
$\frac{80}{0.8g}=\frac{98}{x}$
解得:x=0.98g
稀H2SO4的溶质质量分数为:$\frac{0.98g}{10g}$×100%=9.8%;
故答案为:(1)SO42-;(2)0.8;(3)稀H2SO4的溶质质量分数是9.8%.
点评 此题是一道结合图象的计算题,解题时找到pH=7的恰好反应点,并利用化学方程式的计算进行解决是解题的突破口.

练习册系列答案
相关题目
14.下列图象不能正确反映对应变化关系的是( )
| A. | 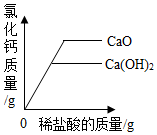 向等质量的氧化钙、氢氧化钙中分别加入等质量分数的稀盐酸至过量 | |
| B. | 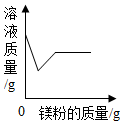 向一定质量氯化亚铁和氯化铝的混合溶液至加入镁粉至过量 | |
| C. |  向盐酸和氯化钙的混合溶液中逐滴加入纯碱溶液至过量 | |
| D. |  向等质量的镁、铝中分别加入等质量分数的稀硫酸至过量 |
10.新型水处理剂ClO3的新制法微观过程如图所示,下列说法正确的是( )


| A. | 乙、丙、丁都是混合物 | B. | 该反应属于置换反应 | ||
| C. | 生成物丙是水 | D. | 该反应符合质量守恒定律 |
20.下列方案一定能达到实验目的是( )
| 选项 | 实验目的 | 实验方法 |
| A | 检验一瓶气体是否为二氧化碳 | 将燃着的木条伸入瓶中 |
| B | 鉴别石灰水和氢氧化钠溶液 | 加入适量的稀盐酸 |
| C | 比较三种金属活动性 | 将锌、银分别放入硝酸铜溶液中 |
| D | 鉴别聚乙烯和聚氯乙烯 | 点燃并在火焰山方各罩一烧杯观察 |
| A. | A | B. | B | C. | C | D. | D |
7.下列试验操作错误的是( )
| A. |  滴加液体 | B. |  添加酒精 | C. |  加热液体 | D. |  检查装置气密性 |
5.近年来,株洲市政府高度重视垃圾分类存放的问题.下列垃圾中不属于有害垃圾的是( )
| A. | 破铜烂铁 | B. | 废旧电池 | C. | 变质药品 | D. | 废荧光灯管 |
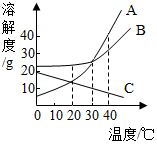 如图所示是A、B、C(均不含结晶水)三种物质的溶解度曲线,回答下列问题.
如图所示是A、B、C(均不含结晶水)三种物质的溶解度曲线,回答下列问题.