题目内容
10.某化合物12克在空气中燃烧生成8.8克二氧化碳和3.6克水,若消秏氧气的质量为8.6克,则该化合物的组成推断正确的是( )| A. | 只含碳,氢两种元素 | B. | 一定含有碳、氢两种元素 | ||
| C. | 一定含有碳、氢、氧三种元素 | D. | 无法确定 |
分析 根据“12克的某化合物在空气中燃烧生成8.8克二氧化碳和3.6克水”和二氧化碳中C元素的质量分数和水中H元素的质量分数,计算出生成物中C元素的质量与H元素的质量,根据质量守恒定律,计算出该物质中O元素的质量,即可判断出该物质中是否一定含有C、H、O元素.
解答 解:生成物中C元素的质量=8.8g×$\frac{12}{44}$=2.4g,
生成物中H元素的质量=3.6g×$\frac{2}{18}$=0.4g,
根据质量守恒定律,该物质中O元素的质量=12.4g-2.4g-0.4g=9.6g,
故选:C.
点评 本题主要考查学生运用质量守恒定律解答问题的能力.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
1.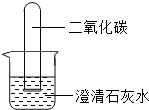 如图所示,将充满CO2的试管倒插入装有澄清石灰水的烧杯中,一段时间后,可能看不到的现象是( )
如图所示,将充满CO2的试管倒插入装有澄清石灰水的烧杯中,一段时间后,可能看不到的现象是( )
 如图所示,将充满CO2的试管倒插入装有澄清石灰水的烧杯中,一段时间后,可能看不到的现象是( )
如图所示,将充满CO2的试管倒插入装有澄清石灰水的烧杯中,一段时间后,可能看不到的现象是( )| A. | 试管中CO2减少 | B. | 试管中液面下降 | ||
| C. | 试管中有有一段浑浊的液柱 | D. | 烧杯中的液面下降 |
18.同种元素的原子和离子相比较,不同的是( )
| A. | 核内质子数目 | B. | 核内中子数目 | C. | 核外电子数目 | D. | 原子核 |