题目内容
2.一氧化碳能在高温下还原铁矿石中的氧化铁.用100吨含Fe2O3为80%的铁矿石练铁.可炼出含铁95%的生铁多少吨?Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.分析 由赤铁矿石的质量、氧化铁的质量分数、生铁中铁的质量分数,根据赤铁矿炼铁的化学方程式可以列式计算出炼出生铁的质量.
解答 解:设可炼出含铁95%的生铁的质量为x.
Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
160 112
100t×80% 95%x
$\frac{160}{112}=\frac{100t×80%}{95%x}$ x≈58.9t
答:可炼出含铁95%的生铁的质量为58.9t.
点评 本题难度不大,考查含杂质物质的化学方程式的计算,注意代入方程式计算的必须是纯物质的质量是正确解答此类题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.某化合物12克在空气中燃烧生成8.8克二氧化碳和3.6克水,若消秏氧气的质量为8.6克,则该化合物的组成推断正确的是( )
| A. | 只含碳,氢两种元素 | B. | 一定含有碳、氢两种元素 | ||
| C. | 一定含有碳、氢、氧三种元素 | D. | 无法确定 |
9.在吃火龙果时尽量不要丢弃内层粉红色的果皮,因为其中含有非常珍贵的花青素(C15H11O6),它可以促进视网膜细胞中的视紫质再生,改善视力,还具有抗辐射的作用.下列关于花青素的说法正确的是( )
| A. | 属于无机化合物 | B. | 氧元素质量分数最小 | ||
| C. | 相对分子质量为287g | D. | 花青素分子由碳、氢、氧原子构成 |
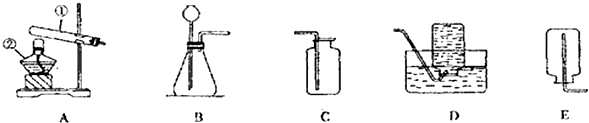
 有下列所示变化:
有下列所示变化: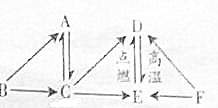 A~F均为九年级化学中的常见物质,它们之间的转化关系如图所示(部分反应物、生成物及反应条件已略去).其中C是空气的主要成分,它是维持人体正常生命活动的重要物质,F为黑色固态非金属单质,根据题给信息回答:
A~F均为九年级化学中的常见物质,它们之间的转化关系如图所示(部分反应物、生成物及反应条件已略去).其中C是空气的主要成分,它是维持人体正常生命活动的重要物质,F为黑色固态非金属单质,根据题给信息回答: