题目内容
10.某学习小组同学用右图实验装置来探究鸡蛋壳里含有CO32-(以CaCO3的形式存在)的可能性,请你一起参与学习探究.【讨论交流】同学们讨论后一致认为若鸡蛋壳里含有CO32-,实验时广口瓶中一定会产生气泡,玻璃片上石灰水会变浑浊,据此写出有气泡生成的化学方程式:CaCO3+2HCl═CaCl2+CO2↑+H2O.
【进行实验】小明和小红在各自的实验中均看到广口瓶中产生气泡,小明还看到玻璃片上石灰水变浑浊,而小红却未看到.他们很好奇,于是进一步探究.
【提出问题】小红的实验中,玻璃片上的石灰水为什么不变浑浊呢?
【做出猜想】小红猜想:可能鸡蛋壳中含有铁等较活泼金属,而不含CO32-;
小明猜想:可能是小红实验所用的盐酸中溶质质量分数过大,挥发出HCl气体.
依据所学化学知识和生活常识,你认为小红的猜想是不合理的.
【实验验证】小红分别取适量等体积的自己实验所用的盐酸a和小明实验中所用用的盐酸b于2试管中,试管内各盛有同一鸡蛋壳的碎片,塞上带导管的橡胶塞,并分别将导管伸入AgNO3溶液中,实验过程如图所示:
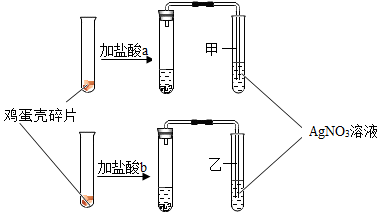
实验中,甲、乙两试管内均有气泡产生,同时甲试管中有白色沉淀生成而乙中没有,白色沉淀的化学式是AgCl.
【实验结论】上述实验说明盐酸a中的溶质的质量分数一定大于(填“大于”或“小于”)盐酸b的质量分数.
【反思应用】(1)实验室制备CO2时,最好选择稀(填“稀”或“浓”)盐酸.
(2)实验中发现,与相同溶质质量分数的盐酸反应时,鸡蛋壳碎片比大块鸡蛋壳更剧烈,说明增大反应物接触面积可以加快反应速率.
分析 【讨论交流】根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳写出有气泡生成的化学方程式;
【做出猜想】根据鸡蛋壳的主要成分是碳酸钙进行分析;
【实验验证】根据氯离子和银离子反应会生成氯化银沉淀进行分析;
【实验结论】根据浓盐酸具有挥发性进行分析;
【反思应用】(1)根据实验室制备CO2时,最好选择稀盐酸进行分析;
(2)根据影响反应速率的因素进行分析.
解答 解:【讨论交流】碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+CO2↑+H2O;
【做出猜想】鸡蛋壳的主要成分是碳酸钙,所以依据所学化学知识和生活常识,认为小红的猜想是不合理的;
【实验验证】氯离子和银离子反应会生成氯化银沉淀,所以白色沉淀的化学式是AgCl;
【实验结论】浓盐酸具有挥发性,所以上述实验说明盐酸a中溶质的质量分数一定大于盐酸b中的溶质的质量分数,同时也说明了鸡蛋壳中含有CO32-的可能性;
【反思应用】(1)由于浓盐酸易挥发出氯化氢气体,所以实验室制备CO2时,最好选择稀盐酸;
(2)实验中发现,与相同溶质质量分数的盐酸反应时,鸡蛋壳碎片比大块鸡蛋壳更剧烈,说明增大反应物接触面积可以加快反应速率.
故答案为:(1)CaCO3+2HCl═CaCl2+CO2↑+H2O;
【做出猜想】小红;
【实验验证】AgCl;
【实验结论】大于;
【反思应用】(1)稀盐酸;(2)接触面积.
点评 在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中的提示进行解答.

练习册系列答案
相关题目
20.下列图示实验操作中,正确的是( )
| A. |  | B. |  | C. |  | D. |  |
5.如表是某研究性学习小组研究影响过氧化氢溶液分解速率的因素时采集的一组数据:用10毫升过氧化氢溶液制取150毫升氧气所需的时间(秒).
请你分析回答:
(1)研究小组在设计方案时,考虑了浓度、等因素对过氧化氢溶液分解速率的影响.写出该反应的文字表达式过氧化氢$\stackrel{一定条件}{→}$水+氧气.
(2)上述影响过氧化氢溶液分解速率的因素中任选一个,说明该因素对分解速率有何影响?浓度越高,过氧化氢的分解速率越快(或温度越高,过氧化氢的分解速率越快;使用催化剂,过氧化氢的分解速率越快..
(3)针对(2)中的因素,设计实验证明该因素对反应速率的影响.简要写出实验步骤、现象、结论.
浓度 反应条件 | 30%的过氧化氢 | 15%的过氧化氢 | 10%的过氧化氢 | 5%的过氧化氢溶液 |
| 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加热 | 360 | 480 | 540 | 720 |
| 二氧化锰作催化剂、加热 | 10 | 25 | 60 | 120 |
(1)研究小组在设计方案时,考虑了浓度、等因素对过氧化氢溶液分解速率的影响.写出该反应的文字表达式过氧化氢$\stackrel{一定条件}{→}$水+氧气.
(2)上述影响过氧化氢溶液分解速率的因素中任选一个,说明该因素对分解速率有何影响?浓度越高,过氧化氢的分解速率越快(或温度越高,过氧化氢的分解速率越快;使用催化剂,过氧化氢的分解速率越快..
(3)针对(2)中的因素,设计实验证明该因素对反应速率的影响.简要写出实验步骤、现象、结论.
2.下列符号中,能表示一个原子、一种元素、一种物质的是( )
| A. | H | B. | N2 | C. | CO | D. | Fe |