题目内容
16.在点燃条件下,甲、乙反应的微观示意图如图.下列说法错误的是( )
| A. | 该反应是氧化反应 | B. | 一定条件下,丁可转化为乙 | ||
| C. | 反应中甲、乙的分子数比为1:1 | D. | 反应中只有氢的化合价不变 |
分析 根据反应的结构示意图和模型表示的原子种类,可判断甲为NH3,乙为O2,丙为N2,丁为H2O,反应的化学方程式为4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O,据此分析有关的问题.
解答 解:由反应的结构示意图和模型表示的原子种类,可判断甲为NH3,乙为O2,丙为N2,丁为H2O,反应的化学方程式为4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O,由此可知:
A、由方程式可知,反应中有氧气的反应,属于特殊的氧化反应;故A说法正确;
B、丁是水,乙是氧气,水通电生成氢气和氧气,故B说法正确;
C、由反应的方程式可知,氨气分子和氧气分子的个数比是4:3,故C说法错误;
D、反应过程中,氮元素的化合价由-3→0,氧元素由0→-2,氢元素的化合价都是+1价,保持不变,故D说法正确;
故选项为:C.
点评 本题以微观模型的形式考查了化学反应,完成此题,首要的是写出反应的化学方程式,然后进行判断.

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
4.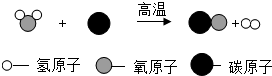 为减少污染、提高煤的利用率,可将其转化为可燃性气体,其微观示意图如图所示,下列说法正确的是( )
为减少污染、提高煤的利用率,可将其转化为可燃性气体,其微观示意图如图所示,下列说法正确的是( )
 为减少污染、提高煤的利用率,可将其转化为可燃性气体,其微观示意图如图所示,下列说法正确的是( )
为减少污染、提高煤的利用率,可将其转化为可燃性气体,其微观示意图如图所示,下列说法正确的是( )| A. | 图中表示化合物的是“ ” ” | |
| B. | 该反应类型为分解反应 | |
| C. | 该反应中反应物两种微粒的个数比为1:1 | |
| D. | 反应前后分子的种类和数目保持不变 |
11.下列化学现象的描述,不正确的是( )
| A. | 加热碳酸氢铵,白色固体逐渐消失,并产生刺激性气味 | |
| B. | 加热碱式碳酸铜,黑色固体变成绿色固体 | |
| C. | 木炭在氧气中燃烧,发出白光并放出大量的热 | |
| D. | 细铁丝在氧气中燃烧,火星四射,生成黑色固体 |
8.“海水晒盐”所获得的粗盐中,除含有泥沙等难溶性杂质外,还含有氯化镁、氯化钙等可溶性杂质,某化学小组为得到较纯净的食盐,进行了下列实验探究活动,请参与他们的探究活动:

【提出问题】如何获得较纯的食盐晶体?
【查阅资料】20℃时,部分物质的溶解性情况如表所示:
【实验方案】按如图方案进行提纯粗盐.
【解释与结论】
(1)操作X的名称是过滤.
(2)沉淀D是碳酸钙.
(3)实验步骤③的主要目的是MgCl2+2NaOH=Mg(OH)2↓+2NaCl (用化学方程式回答);判断氢氧化钠溶液已过量的方法是取溶液B少量于试管中,滴加无色酚酞试液,酚酞试液变红色.
【反思与评价】
(4)有同学认为该实验方案并不完善,其理由及需补充的实验操作是溶液C中还有过量的碳酸钠和氢氧化钠,应该加入适量的稀盐酸反应后再蒸发.

【提出问题】如何获得较纯的食盐晶体?
【查阅资料】20℃时,部分物质的溶解性情况如表所示:
| OH- | CO32- | |
| Na+ | 溶 | 溶 |
| Ca2+ | 微 | 不 |
| Mg2+ | 不 | 微 |
【解释与结论】
(1)操作X的名称是过滤.
(2)沉淀D是碳酸钙.
(3)实验步骤③的主要目的是MgCl2+2NaOH=Mg(OH)2↓+2NaCl (用化学方程式回答);判断氢氧化钠溶液已过量的方法是取溶液B少量于试管中,滴加无色酚酞试液,酚酞试液变红色.
【反思与评价】
(4)有同学认为该实验方案并不完善,其理由及需补充的实验操作是溶液C中还有过量的碳酸钠和氢氧化钠,应该加入适量的稀盐酸反应后再蒸发.

 使用红磷燃烧的方法测定空气中氧气的含量:
使用红磷燃烧的方法测定空气中氧气的含量: