题目内容
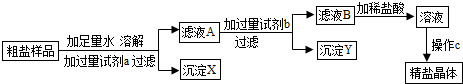
NaCl固体中含有少量CaCl2,欲将CaCl2除去进而配制一定质量分数的NaCl溶液.实验步骤如下图所示:

(1)X的化学式是______.加X过量的目的是______.
(2)加入Y发生反应的化学方程式为______,操作b的名称是______.
解:氯化钙对于氯化钠需要除去的就是钙离子,除去钙离子常用碳酸根离子,有不能引入新的杂质,所以X是碳酸钠溶液,反应后剩余的碳酸钠需要加盐酸除去,所以Y就是盐酸,氯化钠的溶解度受温度的影响变化较小,需要采用蒸发溶解的方法除去,碳酸钠和盐酸反应生成氯化钠、水和二氧化碳;
故答案为:
(1)Na2CO3,除去反应剩余的碳酸钠;
(2)Na2CO3+2HCl=2NaCl+H2O+CO2↑;蒸发.
分析:根据氯化钙对于氯化钠需要除去的就是钙离子,除去钙离子常用碳酸根离子,有不能引入新的杂质,所以X是碳酸钠溶液,加入Y除去剩余的碳酸钠,根据氯化钠的溶解度受温度的影响进行分析.
点评:在解此类题时,首先分析杂质和物质的性质,然后选择适当的试剂只与杂质反应,不与主要物质反应,不会生成新的杂质.
故答案为:
(1)Na2CO3,除去反应剩余的碳酸钠;
(2)Na2CO3+2HCl=2NaCl+H2O+CO2↑;蒸发.
分析:根据氯化钙对于氯化钠需要除去的就是钙离子,除去钙离子常用碳酸根离子,有不能引入新的杂质,所以X是碳酸钠溶液,加入Y除去剩余的碳酸钠,根据氯化钠的溶解度受温度的影响进行分析.
点评:在解此类题时,首先分析杂质和物质的性质,然后选择适当的试剂只与杂质反应,不与主要物质反应,不会生成新的杂质.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 .
.