题目内容
18.漂白粉的主要成分为次氯酸钙[Ca(ClO)2]和氯化钙,即可用作漂白剂,又可用作消毒剂.漂白粉中有效成分是[Ca(ClO)2],漂白的原理是:Ca(ClO)2在空气中发生反应Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO;HClO是一种不稳定,具有漂白性,能使品红等有色物质褪色.(1)漂白粉是一种混合物(填“纯净物”或“混合物”).
(2)HClO在常温下分解,反应为2HClO═2HCl+O2↑.某瓶HClO溶液净重为250g,一段时间后变为232g,则产生的气体的质量为18g
(3)请你计算出HClO中氯元素的化合价为+1.
分析 (1)根据漂白粉的组成考虑;
(2)根据次氯酸分解的产物考虑;根据质量守恒定律分析;
(3)根据化合物中正负化合价代数和为零分析.
解答 解:(1)漂白粉的主要成分为次氯酸钙[Ca(ClO)2]和氯化钙,所以属于混合物;
(2)HClO在常温下分解,反应为2HClO=2HCl+O2↑;HClO溶液净重为250g,一段时间后变为232g,则产生的气体的质量为:250g-232g=18g;
(3)化合物中正负化合价代数和为零,设氯元素的化合价为x,1+x+(-2)=0,x=+1.
故答案为:(1)混合物;
(2)O2;18;
(3)+1.
点评 纯净物与混合物的区别:是否由一种物质组成.

练习册系列答案
相关题目
9.下例叙述不正确的是( )
| A. | 木炭在充足的氧气中燃烧生成二氧化碳 | |
| B. | 硫在充足的氧气中燃烧发出蓝紫色火焰 | |
| C. | 铁丝在充足的氧气中燃烧火星四射,生成三氧化二铁 | |
| D. | 红磷在空气中燃烧产生大量白烟 |
10.要区别空气、氧气和二氧化碳三瓶无色气体,下列方法可行的是( )
| A. | 分别闻三瓶气体的气味 | B. | 加入适量的澄清石灰水 | ||
| C. | 点燃的木条 | D. | 观察三瓶气体的颜色 |
7.发现了元素周期律并编制元素周期表的是( )
| A. | 道尔顿 | B. | 门捷列夫 | ||
| C. | 拉瓦锡 | D. | 阿伏伽德罗和道尔顿 |
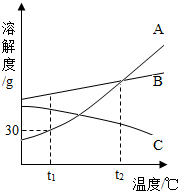 如图是A.B.C三种物质的溶解度曲线,据图回答:
如图是A.B.C三种物质的溶解度曲线,据图回答: