题目内容
4.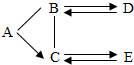 已知A、B、C、D、E是初中化学常见的不同类别的物质.C的水溶液呈蓝色,D是一种红色固体,B→D的反应过程较为复杂,D→B的反应用于冶金工业.中“-”表示相连物质可以发生反应,“→”表示一种物质生成另一种物质(部分反应物、生成物及反应条件省略).
已知A、B、C、D、E是初中化学常见的不同类别的物质.C的水溶液呈蓝色,D是一种红色固体,B→D的反应过程较为复杂,D→B的反应用于冶金工业.中“-”表示相连物质可以发生反应,“→”表示一种物质生成另一种物质(部分反应物、生成物及反应条件省略).(1)D的化学式Fe2O3.
(2)C→E的化学方程式CuSO4+2NaOH═Cu(OH)2↓+Na2SO4,说明该反应能够发生的理由反应物碱和盐都可溶,生成物有沉淀.溶液中发生的一个置换反应方程式Fe+CuSO4=FeSO4+Cu,其微观实质是铁原子和铜离子转变成亚铁离子和铜原子.
分析 根据A、B、C、D、E是初中化学常见的不同类别的物质,C的水溶液呈蓝色,所以C是铜盐,D是一种红色固体,B→D的反应过程较为复杂,D→B的反应用于冶金工业,所以D是氧化铁,所以B是铁,A能够和铁反应,且能够转化为铜盐,所以A是酸,C和E可以相互转化,若C是硫酸铜,则硫酸铜能够和可溶性的碱反应产生氢氧化铜沉淀,然后将推出的物质进行验证即可.
解答 解:(1)A、B、C、D、E是初中化学常见的不同类别的物质,C的水溶液呈蓝色,所以C是铜盐,D是一种红色固体,B→D的反应过程较为复杂,D→B的反应用于冶金工业,所以D是氧化铁,所以B是铁,A能够和铁反应,且能够转化为铜盐,所以A是酸,C和E可以相互转化,若C是硫酸铜,则硫酸铜能够和可溶性的碱反应产生氢氧化铜沉淀,经过验证,推导正确,所以D是铁锈的成分,化学式为:Fe2O3;
(2)C→E的反应可以是硫酸铜和氢氧化钠反应产生氢氧化铜沉淀和硫酸钠的反应,化学方程式为:CuSO4+2NaOH═Cu(OH)2↓+Na2SO4;由于反应物碱和盐都可溶,生成物有沉淀,因此该反应能够发生;溶液中发生的一个置换反应方程式可以是Fe+CuSO4=FeSO4+Cu(或Fe+H2SO4=FeSO4+H2↑);其微观实质是铁原子和铜离子转变成亚铁离子和铜原子(或铁原子转变成亚铁离子,氢离子转变为氢原子,氢原子结合成氢分子).
故答案为:(1)Fe2O3;
(2)CuSO4+2NaOH═Cu(OH)2↓+Na2SO4;反应物碱和盐都可溶,生成物有沉淀;Fe+CuSO4=FeSO4+Cu(或Fe+H2SO4=FeSO4+H2↑);铁原子和铜离子转变成亚铁离子和铜原子(或铁原子转变成亚铁离子,氢离子转变为氢原子,氢原子结合成氢分子).
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

请回答下列问题:
(1)回收塑料可以减少“白色污染”.塑料属于合成材料,下列物质属于合成材料的是D
A.棉花 B.羊毛 C.蚕丝 D.尼龙
(2)焚烧垃圾发电时产生的二氧化硫污染环境,可以用石灰乳吸收,请用化学方程式表示该原理SO2+Ca(OH)2═CaSO3+H2O(已知:二氧化硫与石灰乳反应生成CaS03和水).
(3)沼气化得到的甲烷是一种常用的燃料.
①写出甲烷燃烧的化学方程式CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
②请完成如表实验报告:
| 操作 | 现象 | 结论 |
| 点燃甲烷气体,把用澄清石灰水润湿的烧杯罩在火焰上方 | 烧杯内壁有白色物质出现 | 甲烷中含有碳元素 |
康康选取一定量的含有铜、铝和锌的非铁金属,加人到一定量的AgNO3溶液中,充分反应后过滤.
①若反应后溶液呈蓝色,则向所得固体中滴加稀盐酸没有(填“有”或“没有”)气泡产生.
②若向所得固体中滴加稀盐酸没有气泡产生,则滤液中一定含有哪些溶质(写化学式)Al(NO3)3、Zn(NO3)2?
(5)金属铁的回收利用,一定程度可减少“温室气体”的排放.
工业炼铁时会产生大量的二氧化碳,对环境有一定的影响.如果炼出56t铁,则理论 上排放二氧化碳多少吨?(以赤铁矿为例,其主要成分是氧化铁)
 如图为实验室制取氢气的发生装置,若液面刚好不与锌粒接触面又无酸液可加,要得到氢气且保证H2的量不受影响,可从长颈漏斗中加入适量试剂的一组是( )
如图为实验室制取氢气的发生装置,若液面刚好不与锌粒接触面又无酸液可加,要得到氢气且保证H2的量不受影响,可从长颈漏斗中加入适量试剂的一组是( )①食盐水 ②氢氧化钠溶液 ③氯化钡溶液 ④碳酸钠溶液.
| A. | ①② | B. | ②④ | C. | ①③ | D. | ①④ |
| 实验目的 | 实验方案 | 实验现象及结论 |
| 验证CO2能与NaOH反应 |  | 一段时间后,观察到右侧试管内液面上升较高;由此可验证CO2能与NaOH反应. |
| 验证温度与分子运动的关系 |  | 试管AD中均盛放浓氨水,C中酚酞溶液比B中的酚酞溶液变红的快,烧杯中盛放了一种物质,你认为是热水.结论:温度越高,分子运动越快. |
| 验证铁生锈与O2有关 |  | 一周后,观察到两支铁钉均锈蚀;由此无法验证铁生锈与O2有关.实验改进:为达到实验目的,应对b中实验改进的是在水上方滴一层植物油 |
| A. |  干燥二氧化碳 | B. |  取少量氯化钠 | C. |  二氧化碳验满 | D. |  加热液体 |
| A. | 硬脂酸钠是有机物 | |
| B. | 碳、氢、氧元素的原子个数比为18:35:2 | |
| C. | 硬脂酸钠中钠元素的化合价为+1 | |
| D. | 硬脂酸钠中共含有56个原子 |
 如图是某化肥包装袋上的部分说明:
如图是某化肥包装袋上的部分说明: