题目内容
17.以下物质:①氧气②蒸馏水③新鲜的空气④铜片⑤高锰酸钾(填序号)(1)属于混合物的有③,
(2)属于纯净物的有①②④⑤,
(3)属于单质的有①④,
(4)属于化合物的有②⑤,
(5)属于氧化物的有②.
分析 纯净物由一种物质组成,混合物由两种或两种以上的物质组成;
单质是由一种元素组成的纯净物,化合物是由不同种元素组成的纯净物;
氧化物是由氧元素和另外一种元素组成的化合物.
解答 解:新鲜的空气中含有氮气、氧气等物质,属于混合物;
蒸馏水、氧气、铜和高锰酸钾等物质都是由一种物质组成的,都属于纯净物;
氧气和铜都是由一种元素组成的纯净物,都属于单质;
蒸馏水和高锰酸钾都是由不同种元素组成的纯净物,都属于化合物;
蒸馏水是由氢元素和氧元素组成的化合物,属于氧化物.
故填:③;①②④⑤;①④;②⑤;②.
点评 判断纯净物和混合物时,就是判断物质的物质组成;判断是否是单质、化合物、氧化物时,既要判断元素组成,又要判断物质组成.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案
相关题目
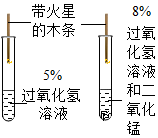
7.以下是某研究小组探究影响反应速率部分因素的相关实验数据.
(1)通过实验①和②对比可知,化学反应速率与双氧水的浓度有关;从实验③和④对比可知,化学反应速率与温度的关系是:在其他条件相同的条件下,温度越高,化学反应速率越大;
(2)化学反应的实质是微观粒子相互接触、碰撞的结果,反应速率与微观粒子的碰撞概率有关.试从微观角度解释“反应物浓度越大,反应温度越高,化学反应速率越大”的原因是:反应物浓度越大,单位体积的反应物中含有的粒子数越多.反应温度越高微粒运动速率越大.这都将使微粒间碰撞的概率增大,导致化学反应速率越大.
| 实验序号 | H2O2溶液 浓度% | H2O2溶液 体积/mL | 反应温度℃ | MnO2的用量/g | 收集氧气的体积/mL | 反应所需 的时间/s |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| ③ | 30 | 5 | 35 | ╱ | 2 | 49.21 |
| ④ | 30 | 5 | 55 | ╱ | 2 | 10.76 |
(2)化学反应的实质是微观粒子相互接触、碰撞的结果,反应速率与微观粒子的碰撞概率有关.试从微观角度解释“反应物浓度越大,反应温度越高,化学反应速率越大”的原因是:反应物浓度越大,单位体积的反应物中含有的粒子数越多.反应温度越高微粒运动速率越大.这都将使微粒间碰撞的概率增大,导致化学反应速率越大.
8.元素观是化学的重要观念之一.下列有关元素的说法错误的是( )
| A. | 物质都是由元素组成的,也都是由分子构成的 | |
| B. | 同种元素的原子核内中子数可能不相同 | |
| C. | 在化学变化中元素的种类不发生改变 | |
| D. | 元素周期表中原子序数等于该元素原子核内的质子数 |
12.过生日时,精美的蛋糕上都会插上漂亮的生日蜡烛,点燃后,让我们吹灭.我们学化学的第一个探究实验也是观察和描述蜡烛的燃烧.如图所示是实验中的几个步骤,请分析下列结论不正确的是( )
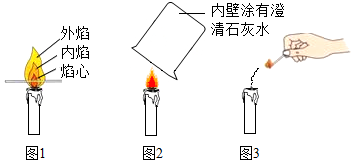

| A. | 实验要先观察物质的物理性质,这是与平时点燃蜡烛的明显不同之处 | |
| B. | 由图1可以清楚地观察到外焰温度最高 | |
| C. | 由图2可见烧杯内澄清的石灰水变浑浊 | |
| D. | 由图3可证明蜡烛是气体燃烧 |
2.如图为某反应前后分子种类变化的微观示意图,其中不同的球代表不同种原子.下列说法中,不正确的是( )


| A. | 分子在化学变化中可分 | |
| B. | 原子在化学变化中不可分 | |
| C. | 此反应一定有单质生成 | |
| D. | 参加反应的两种分子的个数比为1:1 |