题目内容
17. 将氢氧化钠溶液逐滴滴入盐酸和氯化铜的混合溶液中,并根据观察到的现象绘制了如图所示的曲线,根据图示回答问题:
将氢氧化钠溶液逐滴滴入盐酸和氯化铜的混合溶液中,并根据观察到的现象绘制了如图所示的曲线,根据图示回答问题:(1)A点处溶液的溶质是氯化钠和氯化铜.
(2)请写出AB段发生反应的化学方程式CuCl2+2NaOH═Cu(OH)2↓+2NaCl.
分析 根据将氢氧化钠溶液逐滴滴入盐酸和氯化铜的混合溶液中,氢氧化钠溶液先和盐酸反应生成氯化钠和水,当盐酸反应完后氢氧化钠溶液再和氯化铜反应生成氢氧化铜沉淀和氯化钠进行解答.
解答 解:将氢氧化钠溶液逐滴滴入盐酸和氯化铜的混合溶液中,氢氧化钠溶液先和盐酸反应生成氯化钠和水,当盐酸反应完后氢氧化钠溶液再和氯化铜反应生成氢氧化铜沉淀和氯化钠.
(1)A点没有沉淀生成,说明氢氧化钠溶液只和盐酸反应生成氯化钠和水,而氯化铜还没有反应,所以此处溶液的溶质是氯化钠和氯化铜.故填:氯化钠和氯化铜;
(2)AB段是氢氧化钠溶液和氯化铜反应生成氢氧化铜沉淀和氯化钠,发生反应的化学方程式CuCl2+2NaOH═Cu(OH)2↓+2NaCl.故填:CuCl2+2NaOH═Cu(OH)2↓+2NaCl.
点评 本题是图象和化学知识相结合的题型,要求学生有将图象信息转换为化学信息的能力,同时对化学知识必须十分熟练,才可能快速解题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.小林同学取四份50克水后,分别加入一定质量的硝酸钾固体配制成t℃的溶液,充分搅拌后,滤去未溶解的固体,将相关数据记录如表:
根据以上数据,
(1)试判断从第3步骤开始所配制的溶液是饱和溶液;
(2)计算t℃时硝酸钾饱和溶液的溶质质量分数.(结果精确到0.1%)
| 操作序号 | 1 | 2 | 3 | 4 |
| 加入硝酸钾的质量/克 | 40 | 50 | 60 | 70 |
| 溶液的质量/克 | 90 | 100 | 105 | 105 |
(1)试判断从第3步骤开始所配制的溶液是饱和溶液;
(2)计算t℃时硝酸钾饱和溶液的溶质质量分数.(结果精确到0.1%)
5.如表列出了除去物质中所含少量杂质的方法,其中正确的是( )
| 物质 | 所含杂质 | 除去杂质的方法 | |
| A | O2 | CO | 点燃混合气体 |
| B | NaOH | NaCl | 适量的稀盐酸溶液 |
| C | CuO | Cu | 在纯氢气流中加热 |
| D | H2 | 水蒸汽 | 通过盛有浓硫酸的洗气瓶 |
| A. | A | B. | B | C. | C | D. | D |
12.下表是固体甲和乙在不同温度时的溶解度,下列说法中正确的是( )
| 温度/℃ | 0 | 20 | 40 | 100 |
| 甲溶解度/克 | 0.173 | 0.165 | 0.121 | 0.076 |
| 乙溶解度/克 | 13.3 | 31.6 | 63.9 | 246 |
| A. | 20℃时物质的溶解能力大小关系:甲大于乙 | |
| B. | 20℃时100克乙物质加入100克水中,所得溶液的质量是200克 | |
| C. | 100℃时乙物质的饱和溶液冷却到室温会析出晶体后,溶液仍为饱和溶液 | |
| D. | 20℃时甲物质的饱和溶液升高温度会变为不饱和溶液 |
2.如图所示图中,体现稀有气体用途的是( )
| A. |  焊接金属 | B. |  霓虹灯 | C. |  医疗急救 | D. |  灭火 |
9.实验小组用如图的装置进行实验.
请你归纳实验目的:加热氯酸钾和二氧化锰的混合物制取氧气并测量收集氧气的体积.
| 实 验 步 骤 | 简 答 |
(1)称取3g氯酸钾与少量二氧化锰混合后放入装置①的试管中,点燃酒精灯. | 装入药品前要检查装置的气密性 ; 分别用中文名称和化学符号写出a试管中发生反应的表达式:氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气;2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑. |
(2)加热试管一段时间后,再用橡皮管连接a、b;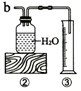 当装置②中水面不再下降,断开a、b,移去酒精灯. | 为什么“加热试管一段时间后,再用橡皮管连接a、b”?原因是:一开始排出的是试管中的空气; ③中使用量筒的作用是通过测量水的体积测量收集的氧气体积. |
7.下列物质由分子构成的是( )
| A. | 氯化钠 | B. | 金属铜 | C. | 干冰 | D. | 金刚石 |
 氢氧化钙长期存放容易变质.某小组在实验时取了一瓶存放多年的氢氧化钙来检查变质情况.取12.2g样品,加入32.8g水,形成悬浊液,然后逐渐滴加29.2%的盐酸充分反应.加入盐酸的质量与锥形瓶中物质的质量关系如图.
氢氧化钙长期存放容易变质.某小组在实验时取了一瓶存放多年的氢氧化钙来检查变质情况.取12.2g样品,加入32.8g水,形成悬浊液,然后逐渐滴加29.2%的盐酸充分反应.加入盐酸的质量与锥形瓶中物质的质量关系如图. 学习化学时可用如图表示某些从属关系,下列选项正确的是( )
学习化学时可用如图表示某些从属关系,下列选项正确的是( )