题目内容
(1)一同学用某种粗盐进行提纯实验,步骤见图.
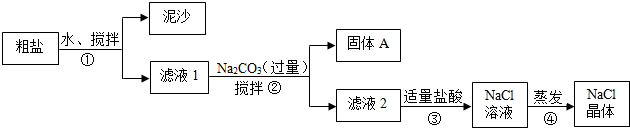
请回答:
(1)步骤①和②的操作名称是 .
(2)步骤③判断加入盐酸“适量”的方法是 ;步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止 ,当蒸发皿中有较多量固体出现时,应 ,用余热使水份蒸干.
(3)猜想和验证:

请回答:
(1)步骤①和②的操作名称是
(2)步骤③判断加入盐酸“适量”的方法是
(3)猜想和验证:
| 猜 想 | 验证的方法 | 现象 | 结论 |
| 猜想Ⅰ:固体A中含CaCO3、MgCO3 | 取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口 | 猜想Ⅰ成立 | |
| 猜想Ⅱ:固体A中含BaCO3 | 取少量固体A于试管中,先滴入 | 有气泡放出,无白色沉淀 |
考点:氯化钠与粗盐提纯,蒸发与蒸馏操作,盐的化学性质
专题:常见的盐 化学肥料
分析:(1)根据粗盐提纯实验的步骤为:溶解→过滤→蒸发结晶进行分析;
(2)根据酸和碳酸盐反应生成气体,玻璃棒的作用以及蒸发过程的注意事项进行分析;
(3)猜想Ⅰ:根据CaCO3、MgCO3与盐酸反应生成二氧化碳进行分析;
猜想Ⅱ:根据碳酸钡和稀盐酸反应生成氯化钡、水和二氧化碳,氯化钡和硫酸钠反应生成白色沉淀硫酸钡进行分析.
(2)根据酸和碳酸盐反应生成气体,玻璃棒的作用以及蒸发过程的注意事项进行分析;
(3)猜想Ⅰ:根据CaCO3、MgCO3与盐酸反应生成二氧化碳进行分析;
猜想Ⅱ:根据碳酸钡和稀盐酸反应生成氯化钡、水和二氧化碳,氯化钡和硫酸钠反应生成白色沉淀硫酸钡进行分析.
解答:解:(1)粗盐提纯步骤为:溶解→过滤→蒸发结晶,步骤①和②都分离出了固体和液体,所以操作名称是:过滤;
(2)因为盐酸和碳酸钠反应生成气体,所以再向溶液中滴加稀盐酸看有无气泡产生即可判断稀盐酸的量;步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止局部过热,造成液滴飞溅;当蒸发皿中有较多量固体出现时,应停在加热,用余热使水分蒸干;
(3)猜想Ⅰ:因为CaCO3、MgCO3与盐酸反应生成二氧化碳,二氧化碳使澄清的石灰水变浑浊,
猜想Ⅱ:因为碳酸钡和稀盐酸反应生成氯化钡、水和二氧化碳,氯化钡和硫酸钠反应生成白色沉淀硫酸钡,由反应现象知,有气泡放出,无白色沉淀,所以没有钡离子存在.
故答案为:(1)过滤;
(2)滴加盐酸至无气泡放出为止,局部过热,造成液滴飞溅,停止加热;
(3)
(2)因为盐酸和碳酸钠反应生成气体,所以再向溶液中滴加稀盐酸看有无气泡产生即可判断稀盐酸的量;步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止局部过热,造成液滴飞溅;当蒸发皿中有较多量固体出现时,应停在加热,用余热使水分蒸干;
(3)猜想Ⅰ:因为CaCO3、MgCO3与盐酸反应生成二氧化碳,二氧化碳使澄清的石灰水变浑浊,
猜想Ⅱ:因为碳酸钡和稀盐酸反应生成氯化钡、水和二氧化碳,氯化钡和硫酸钠反应生成白色沉淀硫酸钡,由反应现象知,有气泡放出,无白色沉淀,所以没有钡离子存在.
故答案为:(1)过滤;
(2)滴加盐酸至无气泡放出为止,局部过热,造成液滴飞溅,停止加热;
(3)
| 猜 想 | 验证的方法 | 现象 | 结论 |
| 有气泡放出,石灰水变浑浊 | |||
| 滴入稀盐酸 | 猜想Ⅱ不成立 |
点评:熟记过滤方法及原理、注意事项;学会猜想和验证,会利用一些标志性的特征:硫酸根会和钡离子形成白色沉淀,且不溶于硝酸.

练习册系列答案
相关题目
以石灰石、纯碱、水为原料制取烧碱的过程中,包含了三个基本反应类型,不涉及的是( )
| A、分解反应 | B、复分解反应 |
| C、化合反应 | D、置换反应 |
下列关于分子、原子的说法中正确的是( )
| A、分子能构成物质,原子不能 |
| B、分子是保持物质性质的最小粒子 |
| C、分子可以再分,原子不能再分 |
| D、分子由原子构成 |
下列说法中错误的是( )
| A、电解水生成氢气和氧气,说明水是由氢元素和氧元素组成的 |
| B、氢气燃烧生成水的反应既是化合反应,也是氧化反应 |
| C、使用二氧化锰作催化剂,不能增加双氧水分解放出氧气的总量 |
| D、鱼类能在水中生存,说明氧气易溶于水 |
对于化学反应A+B=C+D,下列说法中不正确的是( )
| A、A、B为酸和碱,C、D中一定有一种是水 |
| B、若A、B为两种化合物,C、D一定都为化合物 |
| C、若生成物C、D中有一种为单质,则该反应一定是置换反应 |
| D、若生成物C和D分别为两种沉淀,A、B有可能为盐和碱 |
如图所示的实验操作中,错误的是( )
A、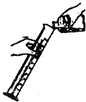 向量桶里倾倒液体 |
B、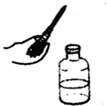 从低瓶里取出液体 |
C、 向试管里加入粉末 |
D、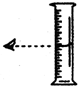 读取量筒内液体体积 |

