题目内容
4.化学兴趣小组同学在实验室中制取CO2,取25g碳酸钙放在烧杯中,然后向其中逐渐加入稀盐酸,使之与碳酸钙充分反应,当碳酸钙恰好完全反应时,加入稀盐酸的质量为90g.请计算:(1)反应生成二氧化碳的质量.
(2)所用稀盐酸中溶质的质量分数.
分析 根据盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,依据碳酸钙的质量和化学方程式中各物质之间的关系计算生成的二氧化碳和参加反应的盐酸质量.
解答 解:设生成二氧化碳的质量为x,参加反应的纯盐酸质量为y,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 44
25g y x
$\frac{100}{25g}$=$\frac{73}{y}$=$\frac{44}{x}$
x=11g
y=18.25g
所以所用稀盐酸中溶质的质量分数为:$\frac{18.25g}{90g}$×100%=20.3%.
答:(1)反应生成二氧化碳的质量是11g;
(2)所用稀盐酸中溶质的质量分数20.3%.
点评 根据化学方程式进行计算时,只能使用纯净物的质量进行计算,而不能把混合物的质量直接代入化学方程式进行计算.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
14.下列资源的利用过程中发生了化学变化的是( )
| A. | 干冰制冷 | B. | 海水晒盐 | C. | 铁矿石炼铁 | D. | 风能发电 |
15.实验是研究和学习化学的重要基础,以下对实验现象的描述正确的是( )
| A. | 将固体碘加入少量的水中,充分溶解后,溶液呈红棕色 | |
| B. | 将氢氧化钠固体放置在空气一段时间,其表面会潮湿 | |
| C. | 将铜锌合金和铜片相互刻划,铜锌合金表面会留有较深的划痕 | |
| D. | 将分别盛有适量的浓氨水和滴有酚酞的蒸馏水的两个小烧杯上方罩上一个大烧杯,过一会,盛有浓氨水的烧杯内溶液呈红色 |
12.王昌龄诗句“留君夜饮对潇湘,从此归来客梦长,岭上梅花侵雪晴,归时还拂桂花香”描述了诗人与好友把盏辞行的情景,下列从微观角度对“归时还拂桂花香”的解释最合理的是( )
| A. | 微粒的体积小,质量轻 | B. | 微粒间有空隙 | ||
| C. | 微粒在不断运动 | D. | 温度越高,微粒运动越快 |
9.下列有关实验操作或现象描述正确的是( )
| A. | 向蛋清溶液中加入饱和的硫酸铵溶液,产生白色沉淀为化学反应 | |
| B. | 用湿润的蓝色石蕊试纸检验氨气时,试纸变为红色 | |
| C. | 用玻璃棒蘸取少量试液滴在湿润的PH试纸上,与标准比色卡对照并读出PH | |
| D. | 碘水滴在馒头片上,出现蓝色 |
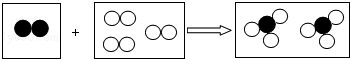
13.如图是某化学反应的微观模型,“ ”、“
”、“ ”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
 ”、“
”、“ ”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
| A. | 该反应属于分解反应 | |
| B. | 反应中共有两种元素参加 | |
| C. | 反应物和生成物中只有一种单质 | |
| D. | 参加反应的两种物质分子个数之比为2:3 |
 如图为A~E物质之间的转化关系,部分转化条件未标出.已知:A为黑色固体单质,B为红色粉末,A、D形成的合金是生产、生活中使用最多的金属材料,甲为常见的气体单质.请按要求完成下列空白:
如图为A~E物质之间的转化关系,部分转化条件未标出.已知:A为黑色固体单质,B为红色粉末,A、D形成的合金是生产、生活中使用最多的金属材料,甲为常见的气体单质.请按要求完成下列空白: .
. 化学与生活、生产密切相关.请回答下列问题:
化学与生活、生产密切相关.请回答下列问题: