题目内容
酸钠和氯化钠组成的固体混合物,向其中逐渐滴加溶质质量分数为10%的稀盐酸(Na2CO3+2HCl=2NaCl+H2O+CO2↑),放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示。请根据题意回答问题:

(1)当滴加了73克稀盐酸时,放出气体的总质量为 克。
(2)当滴加稀盐酸至图中的B点时,烧杯中溶液里的溶质是(写化学式): 。
(3)当滴加了73克稀盐酸时(即A点时),烧杯中为不饱和溶液,试通过计算求出此时所得溶液的溶质的质量分数。(准确到0.1%)
答案:⑴ 4.4 ⑵ NaCl HCl
(3)⑵解:设样品中含a2cO3 为x克,同时生成NaCl为y克
Na2CO3 + 2HCl =2NaCl + H2O+ CO2

106 117 44
x y 4.4
106 117 44


 x = y = 4.4
x = y = 4.4
x=10.6克 y=11.7克
所以 NaCl质量 =11.7+(22.3克-10.6克)
 11.7克+(22.3克-10.6克)
11.7克+(22.3克-10.6克)
所以 NaCl%= (22.3克+73克)——4.4克 = 25.7%
解析:(1)由图象可知,当滴加了73g稀盐酸时,已完全反应,所以设放出气体的总质量为z,根据化学方程式可得737.3=44z,解之得z=4.4g,故放出气体的总质量为4.4g;
(2)因到A点时已完全反应,故到B 点时盐酸有剩余,故烧杯中溶液里的溶质有NaCl、HCl;
(3)烧杯里不饱和溶液中溶质的质量为:11.7g+(22.3g-10.6g)=23.4g
烧杯里不饱和溶液质量为:22.3g+73g-4.4g=90.9g
烧杯里不饱和溶液中溶质的质量分数为:(23.4g÷90.9g)×100%=25.7%
答:其中溶质的质量分数为25.7%.

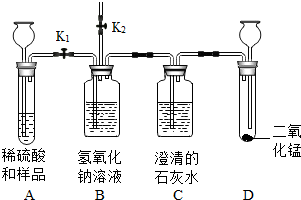
 (2012?丽水)为测定由氯化钙和氯化钠组成的固体样品中氯化钙的含量,某同学进行了如下实验:
(2012?丽水)为测定由氯化钙和氯化钠组成的固体样品中氯化钙的含量,某同学进行了如下实验: