题目内容
 认真分析下列内容,回答相关问题.
认真分析下列内容,回答相关问题.| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
(2)20℃时,将20g NaCl加入50g水中形成溶液的质量为
(3)从海水中提取食盐通常采取晾晒海水的方法,这是因为随温度升高氯化钠的溶解度变化
(4)10℃时,分别在100g 水中加入35g NaCl 和KNO3固体,加热到60℃时,NaCl溶液为
A.10℃时,两溶液中溶质的质量分数相同
B.60℃时,两溶液中溶质的质量分数相同
C.加热前后,NaCl溶液中溶质的质量分数不变
D.加热前后,KNO3溶液中溶质的质量分数不变
(5)如图所示,20℃时,将盛有饱和硝酸钾溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出.加入的物质可能是
A.氢氧化钠 B.生石灰 C.硝酸铵 D.浓硫酸.
考点:固体溶解度的影响因素,溶解时的吸热或放热现象,溶质的质量分数,生石灰的性质与用途,海水晒盐的原理和过程
专题:溶液、浊液与溶解度
分析:(1)依据10℃时硝酸钾的溶解度解决.
(2)根据20℃时氯化钠的溶解度是36g分析解答;
(3)根据随温度升高氯化钠的溶解度变化小解答;
(4)依据加热前后两物质的溶解度变化情况,结合溶液中状态的改变对相关选项进行分析判断即可;
(5)由于硝酸钾的溶解度随温度的升高而明显增大,硝酸钾的饱和溶液中有晶体析出,说明温度降低了,因此加入的物质应是溶于水吸热的物质.
(2)根据20℃时氯化钠的溶解度是36g分析解答;
(3)根据随温度升高氯化钠的溶解度变化小解答;
(4)依据加热前后两物质的溶解度变化情况,结合溶液中状态的改变对相关选项进行分析判断即可;
(5)由于硝酸钾的溶解度随温度的升高而明显增大,硝酸钾的饱和溶液中有晶体析出,说明温度降低了,因此加入的物质应是溶于水吸热的物质.
解答:解:
(1)由于10℃时硝酸钾的溶解度是20.9g,所以此温度下100g水中溶解20.9g硝酸钾溶液恰好达到饱和;
(2)由于20℃时氯化钠的溶解度是36g,所以此温度下100g水中溶解36g氯化钠溶液恰好达到饱和,50g水中溶解18g氯化钠,形成溶液的质量为69g;
(3)从海水中提取食盐通常采取晾晒海水的方法,这是因为随温度升高氯化钠的溶解度变化小;
(4)10℃时,分别在100g 水中加入35g NaCl 和KNO3固体时氯化钠能完全溶解,此时氯化钠是不饱和溶液,硝酸钾不能完全溶解是饱和溶液,加热到60℃时氯化钠仍为不饱和溶液,而硝酸钾剩余固体全部溶解且溶液变成不饱和溶液,所以60℃时,两溶液中溶质的质量相同,因溶剂相同故溶质质量分数相同,对于氯化钠溶液来说加热前后,NaCl溶液中溶质与溶剂的两均未变化,故溶质的质量分数不变;
(5)由于硝酸钾的溶解度随温度的升高而明显增大,硝酸钾的饱和溶液中有晶体析出,说明温度降低了,因此加入的物质应是溶于水吸热的物质,氢氧化钠固体、浓硫酸、生石灰固体溶于水放热,温度升高,均使硝酸钾的溶解度增大,故都不对.故选C.
故答案为:(1)20.9(2)68;(3)小;(4)不饱和;BC;(5)C.
(1)由于10℃时硝酸钾的溶解度是20.9g,所以此温度下100g水中溶解20.9g硝酸钾溶液恰好达到饱和;
(2)由于20℃时氯化钠的溶解度是36g,所以此温度下100g水中溶解36g氯化钠溶液恰好达到饱和,50g水中溶解18g氯化钠,形成溶液的质量为69g;
(3)从海水中提取食盐通常采取晾晒海水的方法,这是因为随温度升高氯化钠的溶解度变化小;
(4)10℃时,分别在100g 水中加入35g NaCl 和KNO3固体时氯化钠能完全溶解,此时氯化钠是不饱和溶液,硝酸钾不能完全溶解是饱和溶液,加热到60℃时氯化钠仍为不饱和溶液,而硝酸钾剩余固体全部溶解且溶液变成不饱和溶液,所以60℃时,两溶液中溶质的质量相同,因溶剂相同故溶质质量分数相同,对于氯化钠溶液来说加热前后,NaCl溶液中溶质与溶剂的两均未变化,故溶质的质量分数不变;
(5)由于硝酸钾的溶解度随温度的升高而明显增大,硝酸钾的饱和溶液中有晶体析出,说明温度降低了,因此加入的物质应是溶于水吸热的物质,氢氧化钠固体、浓硫酸、生石灰固体溶于水放热,温度升高,均使硝酸钾的溶解度增大,故都不对.故选C.
故答案为:(1)20.9(2)68;(3)小;(4)不饱和;BC;(5)C.
点评:溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线中看出的①同一溶质在不同温度下的溶解度;②同一温度下,不同溶质的溶解度;③温度对不同物质的溶解度影响不同等都是解决此类题的关键.

练习册系列答案
相关题目
下列四个坐标示意图分别表示四个实验过程中的某些变化情况,其中正确的是( )
A、 加热一定量碳酸氢钠的实验,试管中固体的质量变化 |
B、 等质量的镁条和铁丝分别与足量的稀硫酸反应,产生气体的质量变化 |
C、 向一定质量的稀盐酸中加入氢氧化钠时,形成的溶液pH的变化 |
D、 向盛有氢氧化钡溶液的烧杯中逐滴滴加稀硫酸,测得烧杯中溶液导电性的变化 |
酸碱中和反应,在日常生活生产中应用广泛.张萌列举的实际应用中,属于利用中和反应原理的是( )
①用碳酸钙与盐酸反应制取二氧化碳
②用小苏打治疗胃酸过多
③用熟石灰改良酸性土壤
④用稀氨水涂抹在蚊子叮咬处(分泌出蚁酸)止痒.
①用碳酸钙与盐酸反应制取二氧化碳
②用小苏打治疗胃酸过多
③用熟石灰改良酸性土壤
④用稀氨水涂抹在蚊子叮咬处(分泌出蚁酸)止痒.
| A、①② | B、②③④ |
| C、③④ | D、①③④ |
我国铁路将进入高铁时代.为适应提速要求需把短轨连成长轨,常用反应:xAl+Fe2O3
Al2O3+xFe 进行焊接,该反应发生后,不需要再持续加热就可保持高温继续进行,方便野外操作.下列说法不正确的是( )
| ||
| A、Al2O3为氧化物 |
| B、该反应方程式中的x为3 |
| C、该反应为置换反应 |
| D、该反应会放出大量热 |
下列物质敞口放置一段时间后,质量不会发生变化的是( )
| A、浓硫酸 | B、氯化钠 |
| C、浓盐酸 | D、澄清石灰水 |
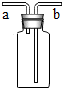 如图有多种功能,如收集气体、洗涤气体、贮存气体等.回答下列问题
如图有多种功能,如收集气体、洗涤气体、贮存气体等.回答下列问题