题目内容
【题目】“鱼浮灵”主要成分是过碳酸钠(xNa2CO3yH2O2),俗称固体双氧水.兴趣小组对其进行以下探究: 【性质探究】
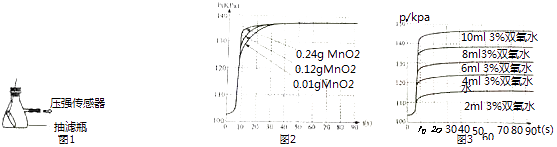
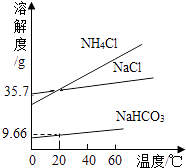
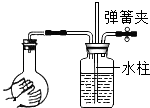
(1)取少量“鱼浮灵”于试管中加水,有持续细小气泡缓慢放出;向试管中加入少量MnO2粉末,产生大量气泡.将带火星木条伸入试管,木条 , 说明有O2生成.
(2)取实验(1)中上层清液,测得溶液pH>7;向溶液中滴加足量稀盐酸,产生大量气泡;将产生的气体通入澄清石灰水中,出现浑浊现象,说明有生成.
(3)结论:过碳酸钠具有Na2CO3和H2O2的双重化学性质. 【工业制备】(如图)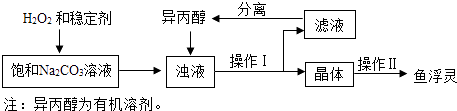
稳定剂的作用是;稳定剂中MgCl2和Na2SiO3发生复分解反应,生成一种难溶物将过碳酸钠粒子包裹住,该反应的化学方程式为 .
(4)浊液中加入异丙醇的作用是 .
(5)操作Ⅱ中洗涤晶体的试剂最好选用(填字母).
A.饱和NaCl溶液
B.水
C.异丙醇
D.稀盐酸
(6)根据如表数据,你认为上述制备反应的最佳温度范围是℃.
温度范围/℃ | 5~10 | 10~15 | 15~20 | 20~25 |
活性氧含量/% | 13.94 | 14.02 | 15.05 | 14.46 |
“鱼浮灵”的产率/% | 85.49 | 85.78 | 88.38 | 83.01 |
注:活性氧含量是指产品中能转化为O2的氧元素的质量分数.
(7)【组成测定】利用如图装置进行产品中活性氧含量测定和过碳酸钠(xNa2CO3yH2O2)组成的测定(杂质对测定无影响). 【查阅资料】①“鱼浮灵”中活性氧含量≥13.0%是一等品,≥10.5%是合格品.
②过碳酸钠能与酸反应放出CO2和O2 . 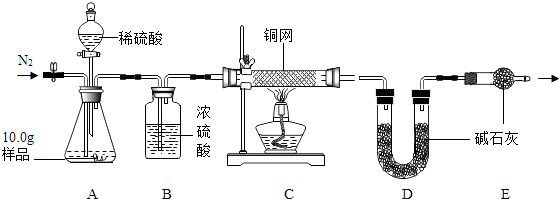
实验前先缓慢通N2一段时间,加热铜网至红热后,再缓慢滴入过量稀硫酸,直至A中样品完全反应;继续缓慢通N2 , 其目的是 .
(8)若先滴入稀硫酸,后加热铜网,会导致x:y的值(填“偏大”或“偏小”).
(9)装置B的作用是(填序号) ①除去气体中的水蒸气 ②便于观察和控制气流速度
(10)实验测得C装置中铜网增重1.2g,D装置增重2.2g.该产品中活性氧含量为%;属于(填“一等品”或“合格品”);x:y= .
【答案】
(1)复燃
(2)CO2(或二氧化碳)
(3)防止H2O2分解(或防止过碳酸钠分解);MgCl2+Na2SiO3=MgSiO3↓+2NaCl
(4)降低过碳酸钠的溶解度(或减少过碳酸钠的溶解或提高产率等)
(5)C
(6)15~20
(7)使残留在装置中的气体全部被装置吸收
(8)偏大
(9)①②
(10)12;合格品;2:3
【解析】解:(1)由结论“说明有O2生成”,再根据:氧气能使带火星的木条复燃,则填复燃;(2)根据题目中信息“将产生的气体通入澄清石灰水中,出现浑浊现象”,再根据:二氧化碳能使带澄清石灰水变浑浊,则此题结论为有 CO2(或二氧化碳)生成.(3)实验中加入稳定剂的作用是为防止H2O2分解(或防止过碳酸钠分解)而失效;稳定剂中的氯化镁MgCl2与硅酸钠Na2SiO3发生复分解反应,能生成氯化钠和难溶的硅酸镁,覆盖在过碳酸钠表面起保护作用,其化学方程式为MgCl2+Na2SiO3=MgSiO3↓+2NaCl.(4)由框图可知,加入异丙醇后经操作Ⅰ后得到的是滤液和晶体,因此操作Ⅰ应该是过滤步骤,由此可知,加入异丙醇的作用是降低过碳酸钠的溶解度(过碳酸钠在有机溶剂中的溶解度较小)以利于其析出晶体,因此浊液中加入异丙醇的作用是降低过碳酸钠的溶解度(或减少过碳酸钠的溶解或提高产率等);(5)因过碳酸钠不溶于异丙醇,所以操作Ⅱ中洗涤晶体最好选用异丙醇;(6)由表中数据可以看出,在15℃~20℃时,活性氧含量最高,鱼浮灵产率最高,所以最好在该温度范围内制备鱼浮灵.(7)实验前通氮气一段时间,加热铜网至红热后,再缓慢滴入过量稀硫酸,直至A中样品完全反应是为了除去装置内的氧气,以防测定值偏高;实验后还要继续通氮气是为了使残留在装置中的气体全部被装置吸收;(8)根据【组成测定】利用如图装置进行产品中活性氧含量测定和过碳酸钠(xNa2CO3yH2O2)组成的测定.若先滴入稀硫酸,后加热铜网,将使部分氧气散逸,计算时过氧化氢相对含量偏小,碳酸钠相对含量偏大,导致x:y的值偏大;(9)装置B的作用是干燥气体,防止水分进入D装置使测定值偏大;同时便于观察和控制气流速度以使反应充分进行,故选①②;(10)C装置中铜网增重1.2g,则说明生成氧气的质量为1.2g,氧气质量占样品的百分数(活性氧含量)为 ![]() =12%大于10.5%而小于13%,“资料中鱼浮灵中活性氧含量≥13.0%是一等品,≥10.5%是合格品”,故此产品属于合格品; 因为生成氧气的质量为1.2g,则设需要过氧化氢的质量为x.
=12%大于10.5%而小于13%,“资料中鱼浮灵中活性氧含量≥13.0%是一等品,≥10.5%是合格品”,故此产品属于合格品; 因为生成氧气的质量为1.2g,则设需要过氧化氢的质量为x.
2H2O2~ | O2↑ |
68 | 32 |
x | 1.2g |
则 ![]() ,解得x=2.55g,故由氧气质量可计算过氧化氢质量为2.55g.
,解得x=2.55g,故由氧气质量可计算过氧化氢质量为2.55g.
因为D装置增重2.2g说明生成二氧化碳2.2g,则设需要碳酸钠质量为y.
Na2CO3~ | CO2 |
106 | 44 |
y | 2.2g |
则 ![]() ,解得y=5.3g,故计算反应的碳酸钠质量为5.3g,
,解得y=5.3g,故计算反应的碳酸钠质量为5.3g,
根据“产品中活性氧含量测定和过碳酸钠(xNa2CO3yH2O2)组成”,则可得:106x:34y=5.3g:2.55g,故解得x:y=2:3.
所以答案是:(1)复燃;(2)CO2(或二氧化碳);(3)防止H2O2分解(或防止过碳酸钠分解),MgCl2+Na2SiO3=MgSiO3↓+2NaCl;(4)降低过碳酸钠的溶解度(或减少过碳酸钠的溶解或提高产率等);(5)C;(6)15~20;(7)使残留在装置中的气体全部被吸收;(8)偏大;(9)①②;(10)12;合格品;2:3.
【考点精析】根据题目的已知条件,利用氧气的检验和验满和书写化学方程式、文字表达式、电离方程式的相关知识可以得到问题的答案,需要掌握氧气的验满:用带火星的木条放在集气瓶口;检验:用带火星的木条伸入集气瓶内;注意:a、配平 b、条件 c、箭号.

 阅读快车系列答案
阅读快车系列答案