题目内容
某厂生产的产品碳酸钠中混有少量碳酸氢钠。为了测定产品中碳酸钠的质量分数,取100g样品加热(2NaHCO3  Na2CO3
+ H2O + CO2↑ ,碳酸钠受热不分解),完全分解生成二氧化碳气体0.22g。求:
Na2CO3
+ H2O + CO2↑ ,碳酸钠受热不分解),完全分解生成二氧化碳气体0.22g。求:
(1)样品中碳酸氢钠的质量。
(2)样品中碳酸钠的质量分数。
【答案】
(1)0.84g;(2)99.16%
【解析】
试题分析:根据碳酸氢钠受热分解的化学方程式,由产生二氧化碳的质量计算分解的碳酸氢钠的质量,样品质量与碳酸氢钠质量的差即样品中碳酸钠的质量,该质量与样品质量比可计算100g混合物中碳酸钠的质量分数。
(1)解:设样品中碳酸氢钠的质量为X
2NaHCO3 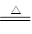 Na2CO3
+ H2O + CO2↑
Na2CO3
+ H2O + CO2↑
168 44
X 0.22g
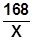 ==
==
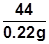
X == 0.84g
(2)碳酸钠的质量分数 = 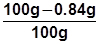 ×100%
== 99.16%
×100%
== 99.16%
答:样品中碳酸氢钠的质量是0.84g;碳酸钠的质量分数是99.16%。
考点:本题考查根据化学反应方程式的计算
点评:此题是对化学方程式计算的考查,解题的关键是找到已知量,此题则是利用反应生成二氧化碳的质量求出其它物质的质量。

练习册系列答案
相关题目


 Na2CO3+______+CO2↑
Na2CO3+______+CO2↑