题目内容
某实验小组为测定铜和氧化铜混合物中氧化铜的质量分数,设计了用干燥纯净的氢气还原氧化铜的实验,所需实验装置如图所示,回答下列问题:
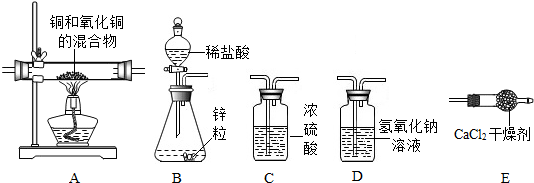
(1)将上图连接成整套装置,连接顺序依次为B→ → → →E(填写字母).
(2)A装置中实验前混合物质量为2.5g,实验后的剩余固体质量为2.1g,则混合物中的质量分数为 .
(3)某同学用E装置增加的质量来计算混合物中氧化铜的质量分数,计算的结果会 (填“增大”、“减少”或“不变”)

(1)将上图连接成整套装置,连接顺序依次为B→
(2)A装置中实验前混合物质量为2.5g,实验后的剩余固体质量为2.1g,则混合物中的质量分数为
(3)某同学用E装置增加的质量来计算混合物中氧化铜的质量分数,计算的结果会
考点:实验探究物质的组成成分以及含量,气体的净化(除杂),氢气的制取和检验,氢气的化学性质与燃烧实验
专题:科学探究
分析:(1)按照要求需要制取、除杂、干燥、还原、吸收的步骤分析;
(2)根据氯化钙增重的原因分析误差;
(3)根据反应前后固体减少的质量就是参加反应的氧化铜中氧元素的质量计算出氧化铜的质量,从而再计算氧化铜的质量分数.
(2)根据氯化钙增重的原因分析误差;
(3)根据反应前后固体减少的质量就是参加反应的氧化铜中氧元素的质量计算出氧化铜的质量,从而再计算氧化铜的质量分数.
解答:解:(1)要用干燥纯净的氢气还原氧化铜,要求制取的气体显除杂(氢氧化钠溶液学生氯化氢)再干燥(浓硫酸吸水),然后通过氧化铜装置发生还原反应,用氯化钙吸水产物水,故连接装置的顺序为:B→D→C→A→E;
(2)实验前混合物质量为2.5g,实验后的剩余固体质量为2.1g,减少了0.4g就是氧化铜中氧元素的质量,故氧化铜的质量为:0.4g/(
×100%)=2g,
故氧化铜的质量分数为:
×100%=80%.
(3)氯化钙吸收的水分来自反应的产生的水和空气中的水,因此结果会偏大;
故答案为 (4)D→C→A (5)80% (6)增大.
(2)实验前混合物质量为2.5g,实验后的剩余固体质量为2.1g,减少了0.4g就是氧化铜中氧元素的质量,故氧化铜的质量为:0.4g/(
| 16 |
| 80 |
故氧化铜的质量分数为:
| 2g |
| 2.5g |
(3)氯化钙吸收的水分来自反应的产生的水和空气中的水,因此结果会偏大;
故答案为 (4)D→C→A (5)80% (6)增大.
点评:本题考查了气体制取装置的气密性检验、收集、除杂、干燥及相关的计算,可依据题干的信息结合已有的化学知识完成.

练习册系列答案
相关题目
联合国确定2014年“世界水日”的宣传主题是“水与能源(Water and Energy)”.我国纪念2014年“世界水日”和“中国水周”活动的宣传主题为“加强河湖管理,建设水生态文明”.下列做法中符合这一主题的是( )
| A、保护水资源,禁止使用农药化肥 |
| B、利用沉降的方法将硬水转化为软水 |
| C、富含氮、磷的生活污水直接排放 |
| D、城市浇花使用喷灌、滴灌技术 |
下列方法能直接从海水制取可饮用水的是( )
| A、萃取 | B、结晶 | C、蒸馏 | D、过滤 |

 如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答:
如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答: